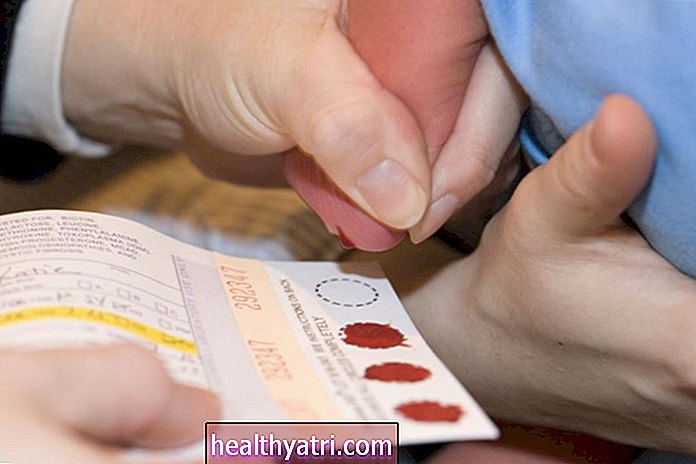
Naarmate gevallen van nieuw coronavirus (COVID-19) toenemen in een voorspelde winterse stijging, staat een aantal vaccins in de pijplijn om een einde te maken aan de pandemie. Een daarvan is het vaccin van Moderna, mRNA-1273 genaamd. Het vaccin van Moderna is het tweede vaccin dat voor noodgevallen toestemming heeft gekregen van de Amerikaanse Food and Drug Administration (FDA).
zoranm / Getty ImagesModerna, een Amerikaans biotechnologiebedrijf gevestigd in Cambridge, Massachusetts, begon in januari 2020 met de ontwikkeling van zijn vaccin. Het bedrijf werkte samen met de National Institutes of Health (NIH) om de gensequentiebepaling voor het virus af te ronden en begon kort daarna aan de ontwikkeling van het vaccin.
De eerste batch van het vaccin werd begin februari ontwikkeld - slechts 25 dagen nadat de sequentie van het gen was bepaald. De eerste dosis van het vaccin werd in maart 2020 gegeven in een fase 1 klinische studie, en die vroege studies lieten veelbelovende resultaten zien. Halverwege het jaar ontving Moderna financiering en versnelde wettelijke toelagen om de ontwikkeling vooruit te helpen.
Hoewel een vaccin aanvankelijk 18 maanden of langer niet werd verwacht, zorgden de nieuwe ontwikkelingen ervoor dat Moderna veel eerder miljoenen doses kon afgeven. In augustus 2020 bestelde de Amerikaanse overheid 100 miljoen doses van het vaccin - ook al was het nog niet eens goedgekeurd voor gebruik, en in november werden de resultaten van de klinische fase 1-studie gepubliceerd.
In december werden de resultaten van klinische fase 3-onderzoeken gepubliceerd en bestelden de VS nog eens 100 miljoen doses.
Wanneer werd het vaccin van Moderna officieel goedgekeurd?
Amerikaanse gezondheidsfunctionarissen hebben op 18 december een vergunning voor gebruik in noodgevallen verleend aan het vaccin van Moderna voor volwassenen van 18 jaar en ouder, waardoor het het tweede vaccin is dat binnen een week de benaming van Amerikaanse gezondheidsfunctionarissen krijgt.
Hoe het werkt
Het Moderna-vaccin is een mRNA-vaccin, vergelijkbaar met het vaccin dat door Pfizer is ontwikkeld. De technologie achter deze vaccins bestaat al ongeveer drie decennia en is veelbelovend gebleken bij het voorkomen van notoir moeilijk te voorkomen ziekten - zelfs kanker. In tegenstelling tot conventionele vaccins die geïnactiveerde of levende virussen gebruiken, zijn mRNA-vaccins niet-infectieus en bevatten ze geen delen van het virus dat ze bestrijden. Dit maakt mRNA-vaccins veiliger voor bepaalde populaties.
Een mRNA-vaccin (messenger ribonucleïnezuur) is een enkelstrengs molecuul dat een aanvulling vormt op een streng van uw DNA. Deze strengen hebben een speciale coating die mRNA kan beschermen tegen chemicaliën in het lichaam die het kunnen afbreken en het kunnen helpen de spiercellen binnen te dringen.
In plaats van het lichaam bloot te stellen aan een kleine hoeveelheid virus om een immuunrespons op te wekken, zorgt mRNA ervoor dat de ontvanger van het vaccin het gewenste eiwit maakt. Dit bevat:
- De cel helpen een deel te maken van het verrijkte eiwit dat COVID-19 zo krachtig maakt
- Immuuncellen leren om soortgelijke verrijkte eiwitten te herkennen en te bestrijden
Volgens de Centers for Disease Control and Prevention (CDC) leren mRNA-vaccins onze cellen hoe ze een eiwit kunnen maken - of zelfs maar een stukje van een eiwit. Dit veroorzaakt een immuunrespons.
Het vaccin van Moderna werd aanvankelijk getest bij volwassenen van 18 tot 55 jaar. In de fase 1-studie werden drie verschillende doses onderzocht - 25, 100 en 250 microgram - tweemaal toegediend, 28 dagen na elkaar. Bij de fase 3-studie richtte Moderna zich op een formule van twee doses van elk 100 microgram, gegeven in twee doses met een tussenpoos van ongeveer vier weken.
Hoe werd het vaccin van Moderna getest?
In de fase 3-studie van Moderna werd een vaccin met twee doses (elk 100 microgram, met een tussenpoos van 28 dagen) getest bij volwassenen van 18 jaar en ouder. De proef had meer dan 30.000 deelnemers, waaronder ongeveer 7.500 volwassenen van 65 jaar en ouder en meer dan 5.000 volwassenen van 18 tot 64 jaar met risicofactoren voor ernstige ziekte door COVID-19.
Hoe effectief is het?
Onderzoekers die de proeven hebben uitgevoerd, waren in staat om te testen hoe effectief het vaccin is bij het maken van antilichamen en het neutraliseren van reacties met tests die lichaamsvloeistoffen zoals bloed of urine gebruiken om te zien of er antilichamen tegen een bepaald virus kunnen worden gevonden. Deze tests omvatten:
- ELISA-test (enzymgekoppelde immunosorbent-test)
- PsVNA (pseudotype lentivirus reporter single-round-of-infectie neutralisatietest)
- PRNT (neutralisatietest voor plaque-reductie)
De antilichaamspiegels van deze tests werden vergeleken met die gevonden bij mensen die hersteld waren van COVID-19-infecties. De studie onderzocht ook de reacties van andere immuuncellen, zoals T-cellen.
Na de eerste vaccinatieronde in de 100 microgram- en 250 microgram-formules in de fase 1-studie waren de antilichaamresponsen vergelijkbaar met het mediane niveau van immuniteit bij degenen die hersteld waren van en natuurlijke immuniteit hadden na een COVID-19-infectie.
Andere immuniteitstests, zoals de PsVNA, lieten weinig respons zien na de eerste dosis. Na de tweede dosis waren de antilichaam- en andere immuunresponsen echter sterk onder de vaccinatiegroep, waarbij niveaus werden bereikt die dicht bij die met de hoogste immuunresponsen lagen bij degenen die hersteld waren van COVID-19.
Immuunresponsen ontwikkelden zich binnen ongeveer twee weken na de eerste dosis, volgens het onderzoeksrapport, maar waren veel sterker na de tweede dosis.
Hoe effectief is het precies?
In onderzoeken is aangetoond dat het vaccin van Moderna zeer effectief is: het voorkomt COVID-19 bij 94,1% van de mensen die deelnamen aan het klinische fase 3-onderzoek. Bovendien lijkt het vaccin een brede werkzaamheid te hebben, met succespercentages die consistent zijn over verschillende leeftijds-, ras-, etniciteits- en geslachtsgroepen.
De levensduur van deze vaccins is nog niet duidelijk, maar de leiders van de proef zeggen dat ze het eerste jaar na vaccinatie bloedmonsters van de studiegroep zullen blijven verzamelen om te controleren op immuniteit. In het verleden genereerden virussen in dezelfde virusfamilies geen langdurige immuunresponsen, merkt het onderzoeksrapport op.
Wanneer is het beschikbaar?
Moderna heeft op 18 december toestemming gekregen van de FDA voor zijn vaccin.
Distributie is misschien een beetje gemakkelijker voor Moderna dan Pfizer, omdat het vaccin 30 dagen bij standaard koelkasttemperaturen kan worden bewaard of gedurende zes maanden bij ongeveer -20 graden Celsius kan worden ingevroren. Het Pfizer-vaccin moet bij veel koudere temperaturen worden bewaard.
Wat de kosten betreft, kondigde Moderna tijdens een interne telefonische vergadering in augustus aan dat het vaccin tussen de $ 32 en $ 37 per dosis zou kunnen kosten, maar de uiteindelijke prijzen kunnen veranderen wanneer de ergste pandemie voorbij is.
Volgens de CDC zullen doses van de vaccins die door de Amerikaanse overheid zijn gekocht, echter gratis beschikbaar zijn voor burgers.
Naast de 200 miljoen doses die al door de Amerikaanse overheid zijn besteld, heeft het de optie om er nog eens 300 miljoen aan te schaffen.
Op 26 januari had Moderna 30,4 miljoen doses aan de VS geleverd en 10,1 van deze doses waren volgens het bedrijf toegediend. Moderna kondigde ook aan dat het op schema ligt om eind maart 100 miljoen doses aan de VS af te leveren en de extra 100 miljoen doses eind juni.
Het bedrijf heeft ook afspraken gemaakt om het vaccin aan verschillende andere landen te leveren, waaronder:
- Europese Unie: 80 miljoen eerste doses met een optie voor nog eens 80 miljoen doses
- Japan: 50 miljoen doses
- Canada: 40 miljoen doses met een optie voor nog eens 16 miljoen
- Zwitserland: 7,5 miljoen doses
- Verenigd Koninkrijk: 7 miljoen doses
- Israël: 6 miljoen doses
Een aantal andere landen heeft volgens Moderna ook bestellingen bij het bedrijf geplaatst, maar het aantal bestelde doses is niet bekendgemaakt.
Hoewel het vaccin zelf gratis is als het door de overheid wordt gekocht, kunnen er kosten in rekening worden gebracht door vaccinleveranciers die het vaccin toedienen. Vergoedingsprogramma's voor deze administratieve kosten moeten beschikbaar zijn via zowel openbare als particuliere verzekeringsplannen, evenals via het Provider Relief Fund van de Health Resources and Services Administration voor mensen zonder openbare of particuliere ziektekostenverzekering.
COVID-19-vaccins: blijf op de hoogte van de beschikbare vaccins, wie ze kan krijgen en hoe veilig ze zijn.
Wie kan het Moderna-vaccin krijgen?
Nu vaccins onderweg zijn, is de vraag wie ze krijgt en wanneer? De CDC verwachtte beperkte voorraden in de beginfase van het vaccinatieprogramma, en aanbevelingen voor wie het vaccin het eerst zou moeten krijgen, werden in december 2020 gedaan door CDC's Advisory Committee on Immunization Practices (ACIP) op basis van eerdere richtlijnen van de National Academies of Sciences, Engineering , en geneeskunde.
In termen van het bevel besloten federale gezondheidsfunctionarissen dat gezondheidswerkers en mensen die in instellingen voor langdurige zorg wonen de eersten moesten zijn die de eerste vaccins zouden ontvangen, die aanvankelijk beperkt waren naarmate de productie toeneemt.
Volgens de CDC zijn er meer dan 18 miljoen zorgverleners in de VS en leven ongeveer 1,3 miljoen Amerikanen in instellingen voor langdurige zorg. Elk van deze mensen zou twee doses van de beste vaccinatiekandidaten tot dusver moeten krijgen, in totaal bijna 40 miljoen doses die nodig zijn voor de beginfase van de vaccinatie. De CDC schat dat het enkele maanden zal duren voordat het aanbod van vaccins de vraag kan opvangen.
Richtlijnen over wie het vaccin zal krijgen en wanneer zullen worden beslist zodra er voorraden beschikbaar komen. Alleen al in de VS wonen ongeveer 330 miljoen mensen - wat betekent dat er bijna 700 miljoen vaccindoses nodig zullen zijn om heel Amerika te vaccineren, aangezien andere vaccins een dosis van twee vaccins volgen.
Hoewel er nog weinig informatie beschikbaar is over de details van wanneer iedereen de vaccinatie zal krijgen en waar ze die kunnen krijgen, zullen de nationale en lokale gezondheidsafdelingen de inspanningen coördineren om doses van de vaccins te verdelen zodra deze beschikbaar komen. Het vaccin moet zowel in artsenpraktijken als in winkels verkrijgbaar zijn, zoals apotheken die andere vaccins toedienen.
Het Moderna-vaccin wordt gegeven in twee doses met een tussenpoos van 28 dagen. De CDC beveelt aan om de tweede dosis zo dicht mogelijk bij de 28 dagen te geven, maar kent een uitstelperiode van vier dagen toe wanneer deze iets eerder kan worden gegeven en staat toe dat de tweede dosis in gevallen binnen 42 dagen na de eerste dosis wordt gegeven. waar het 28-dagenvenster niet haalbaar is.
Wanneer zullen kinderen het vaccin kunnen krijgen?
Kinderen zullen het vaccin in eerste instantie niet krijgen, aangezien proeven alleen bij volwassenen zijn uitgevoerd. Moderna begon in december met het werven van deelnemers voor een klinische proef bij 12- tot 17-jarigen. Proeven voor jongere kinderen bevinden zich nog in de planningsfase. Kinderen en tieners kunnen het vaccin later in 2021 krijgen.
Bijwerkingen en bijwerkingen
Mensen die aan het onderzoek deelnamen, werd gevraagd om eventuele reacties op het vaccin te noteren, hetzij op het gebied waar het vaccin werd geïnjecteerd, hetzij die ze in het algemeen ervoeren. Pijn op de plaats waar het vaccin werd geïnjecteerd en algehele vermoeidheid waren de meest voorkomende bijwerkingen in de fase 3-studie.
Systemische effecten zijn reacties die het hele lichaam aantasten, en hoofdpijn en vermoeidheid stonden bovenaan die lijst en kwamen het meest voor in de vaccingroep. Minder dan 20% van de mensen die zijn gevaccineerd, meldt koorts na de tweede dosis.
Lokale effecten hebben daarentegen slechts betrekking op een klein, beperkt gebied. Het meest voorkomende effect in deze categorie was pijn op de injectieplaats.
De ernst van de reacties nam toe met de tweede dosis van het vaccin. Er waren maar weinig reacties die bij de eerste dosis van het vaccin als ernstig werden beoordeeld, maar verscheidene werden na de tweede dosis als ernstig beoordeeld. De meest voorkomende reacties die door deelnemers werden gemeld na de tweede dosis van het vaccin waren:
- Pijn op de injectieplaats
- Vermoeidheid
- Hoofdpijn
- Spierpijn
- Rillingen
- Gewrichtspijn
Misselijkheid of braken, koorts, rode of gezwollen plekken op de injectieplaats en gezwollen of vergrote lymfeklieren werden ook gemeld.
Het percentage ernstige bijwerkingen was hetzelfde voor de placebo- en vaccingroep (0,6%) en duidde niet op bezorgdheid over de veiligheid. Er was in de onderzoeken ook geen bewijs van een met vaccin geassocieerde versterkte ademhalingsziekte. Eerdere vaccins voor coronavirus in diergeneeskundig gebruik en diermodellen hebben geleid tot ademhalingsproblemen in verband met vaccinatie.
Naarmate de tijd verstrijkt, zal er meer observatie worden gedaan bij de studiegroepen, en er zijn meer studies gepland voor speciale populaties, zoals kinderen.
Financiering en ontwikkeling
Moderna werkte samen met de National Institutes of Health en het Amerikaanse ministerie van Volksgezondheid en Human Services om het vaccin te ontwikkelen. Het bedrijf ontving ongeveer $ 1,6 miljard aan federale financiering via de Biomedical Advanced Research and Development Authority (BARDA), een programma van de Amerikaanse overheid om de productie en distributie van vaccins ter bestrijding van COVID-19 te versnellen. nog eens 100 miljoen doses van Moderna voor ongeveer $ 1,68 miljard.


.jpg)












.jpg)