Heel goed / Vincent Iannelli
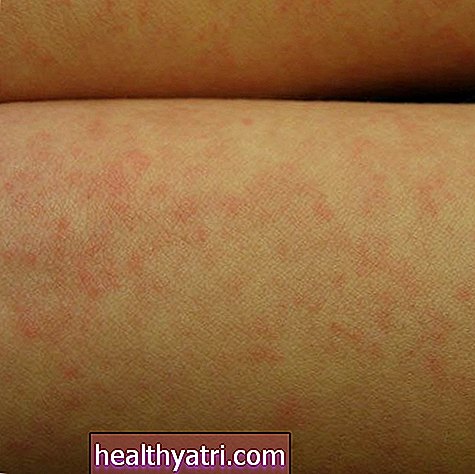
Advair (fluticason + salmeterol) is een inhalatiemedicijn dat wordt gebruikt voor de behandeling van astma en chronische obstructieve longziekten (COPD), waaronder emfyseem en / of chronische bronchitis.
Advair kreeg in 2003 een black box-waarschuwing van de Amerikaanse Food and Drug Administration (FDA) die adviseerde dat salmeterol mogelijk het risico op levensbedreigende astma-aanvallen zou kunnen verhogen. De black box-waarschuwing is in december 2017 verwijderd. Ontdek waarom.
Black Box-waarschuwingen begrijpen
Een black box-waarschuwing is een voorzorgsverklaring van de FDA om het publiek te informeren dat een medicijn ernstige of levensbedreigende schade kan veroorzaken. De "zwarte doos" verwijst letterlijk naar de vetgedrukte doos op de verpakkingsinformatie die het FDA-advies bevat.
Black box-waarschuwingen worden meestal uitgegeven vanwege resultaten van klinische onderzoeken die kunnen worden uitgevoerd nadat het medicijn al is goedgekeurd en beschikbaar is gesteld. Als er ernstige veiligheidsproblemen ontstaan nadat een medicijn al is goedgekeurd, zal de FDA opdracht geven tot onmiddellijke herziening van de verpakkingsinformatie. Mediaberichten zullen ook worden verspreid om het publiek te waarschuwen voor de zorgen.
FDA-zorgen over Advair
In 2003 ontdekte een klinische studie genaamd de Salmeterol Multicenter Asthma Research Trial (SMART) dat salmeterol verband hield met een kleine maar significante toename van het risico op overlijden en ziekenhuisopname bij mensen met astma, met name bij Afro-Amerikanen. Als resultaat van de bevindingen werd een black box-waarschuwing afgegeven met betrekking tot alle medicijnen die salmeterol bevatten, inclusief Advair.
De studie rapporteerde verder een vergelijkbaar risico op overlijden en ziekenhuisopname met formoterol, een medicijn dat tot dezelfde klasse van geneesmiddelen behoort die bekend staat als langwerkende bèta-agonisten (LABA's).
Als ze alleen worden gebruikt, bieden LABA's geen adequate verlichting van de symptomen. Bovendien kunnen LABA's, als ze alleen worden gebruikt, astma-aanvallen veroorzaken.
Het is om deze reden dat co-geformuleerde geneesmiddelen zoals Advair, die ook een inhalatiecorticosteroïde (ICS) bevatten, voor het eerst werden gemaakt.
Bij gebruik met een ICS kunnen de nadelige effecten van LABA's grotendeels worden beperkt.
Toen de studie later werd herzien, werd onthuld dat personen die een LABA met een ICS gebruikten, niet meer of minder risico liepen op overlijden of ziekenhuisopname dan degenen die alleen een corticosteroïd gebruikten. De meeste onderzoekers erkennen tegenwoordig dat de SMART-studie slecht was opgezet en factoren uitsluit die de anomalie anders zouden kunnen verklaren.
Wat de FDA vandaag zegt
In 2016 werd de eerste in een nieuwe ronde van Advair-onderzoeken die door de FDA waren gemandateerd, vrijgegeven.
De AUSTRI-studie evalueerde de veiligheid van fluticason alleen versus combinatie salmeterol en fluticason bij 11.679 mensen met astma, van wie sommigen nog maar 12 jaar waren. gerelateerd aan ras.
De onderzoekers ontdekten dat het risico op astma-aanvallen of andere bijwerkingen niet groter was voor deelnemers die salmeterol-fluticason gebruikten dan voor degenen die alleen fluticason (een corticosteroïde) gebruikten.
De studie bevestigde dat Advair, door een LABA en corticosteroïde in een enkel product af te geven, geen van de risico's opleverde die worden gesuggereerd in de FDA black box-waarschuwing.
Hoewel de FDA een black box-waarschuwing handhaaft voor producten die alleen LABA's gebruiken, bevatten medicijnen die zowel een ICS als LABA bevatten eenWaarschuwing en voorzorgsmaatregelgebruikers herinneren aan de risico's van het gebruik van LABA'szondereen ICS. Geneesmiddelen die zowel een ICS als een LABA bevatten, zijn door de FDA goedgekeurd voor de behandeling van astma en COPD.