Heplisav-B is een vaccin dat wordt gebruikt om alle subtypes van hepatitis B te voorkomen.Het werd op 9 november 2017 goedgekeurd door de Amerikaanse Food and Drug Administration (FDA) voor gebruik bij volwassenen van 18 jaar en ouder.
Het is een van de drie vaccins die momenteel in de Verenigde Staten worden gebruikt om infectie door het hepatitis B-virus (HBV) te voorkomen. Deze omvatten Recombivax HB, dat in 1986 door de FDA werd goedgekeurd, en marktleider Engerix-B, die in 2007 een vergelijkbare goedkeuring kreeg. (Er is ook een derde combinatievaccin, bekend als Twinrix, dat vaccineert tegen zowel hepatitis A als B .)
Een van de belangrijkste voordelen van Heplisav-B is dat het minder injecties vereist gedurende een kortere periode, een factor die mensen kan helpen de serie af te maken in plaats van te stoppen.
Universal Images Group / Universal Images Group / Getty Images
Eerste bezorgdheid over de veiligheid
De goedkeuring van Heplisav-B maakte een einde aan een strijd van vier jaar om het vaccin op de markt te brengen. De FDA had het medicijn eerder in februari 2013 en later in november 2016 afgewezen vanwege bezorgdheid over de veiligheid met betrekking tot het mogelijke risico op een acuut myocardinfarct (hartaanval) en bepaalde auto-immuunziekten.
Het vaccin werd uiteindelijk goedgekeurd, grotendeels gebaseerd op het feit dat er twee injecties nodig zijn die een maand na elkaar worden afgeleverd. De andere vaccins vereisen daarentegen drie injecties met een tussenpoos van één maand en vervolgens zes maanden.
Dit werd als belangrijk beschouwd omdat een van de grootste belemmeringen voor HBV-vaccinatie de therapietrouw was. Een studie uit 2008 door het Department of Infectious Disease aan de Universiteit van Florida in Jacksonville meldde dat van de 707 mensen die in aanmerking kwamen voor HBV-vaccinatie, er slechts 503 toegang kregen tot de behandeling en dat slechts 356 de serie met drie opnames voltooiden. Andere studies hebben vergelijkbare sombere resultaten gerapporteerd.
Door de kloof tussen injecties te verkleinen, is de FDA van mening dat de voordelen van het vaccin veel groter zijn dan de mogelijke gevolgen.
Effectiviteit
De goedkeuring van Heplisav-B was gebaseerd op gegevens van drie klinische onderzoeken met meer dan 14.000 volwassen deelnemers. In het hoofdonderzoek werd een kuur met twee doses Heplisav-B vergeleken met een reeks van drie doses Engerix-B. Van de 6.665 deelnemers die bij het onderzoek betrokken waren, behaalde 95% een hoge mate van bescherming tegen Heplisav-B (gemeten aan de hand van antilichaamactiviteit) vergeleken met 81% bij Engerix-B.
In een tweede onderzoek onder 961 mensen met diabetes type 2 (waarvan wordt aangenomen dat ze een hoog risico op hepatitis B lopen), werd gemeld dat Heplisav-B een hoge mate van bescherming bood bij 90% van degenen die het vaccin kregen, versus slechts 65% bij degenen die Engerix kregen. -B.
Bovendien is bekend dat Heplisav-B bescherming biedt tegen alle vier de belangrijkste serotypen, tien genotypen (A tot en met J) en 40 subgenotypen.
Administratie
Heplisav-B wordt toegediend via intramusculaire injectie in de bovenste deltaspier van de schouder. Het vaccin is geen levend vaccin (dat levend, verzwakt virus bevat) maar bevat in plaats daarvan een genetisch gemodificeerd antigeen - in wezen een avatar voor het virus - dat geen ziekte veroorzaakt maar eerder een beschermende immuunrespons stimuleert.
Nadat u de eerste injectie van 0,5 milliliter (ml) heeft gekregen, wordt er binnen zes maanden een tweede toegediend.
Als u, om welke reden dan ook, de serie niet binnen die tijd kunt voltooien, overleg dan met uw arts om de serie zo snel mogelijk af te ronden. Het is onwaarschijnlijk dat u de serie opnieuw moet starten.
Bijwerkingen
Hoewel sommige mensen een reactie op de injectie kunnen ervaren, zijn de meeste gevallen mild en verdwijnen ze binnen een paar dagen. Over het algemeen zijn de reacties, indien aanwezig, meestal dieper na het eerste schot en minder na het tweede.
De meest voorkomende symptomen (komen voor bij meer dan 2% van de patiënten) zijn:
- Zwelling op de injectieplaats: 2,3%
- Roodheid op de injectieplaats: 4,1%
- Malaise: 9,2%
- Hoofdpijn: 16,9%
- Vermoeidheid: 17,4%
- Pijn op de injectieplaats: 38,5%
Contra-indicaties
Heplisav-B mag niet worden gebruikt bij personen met een voorgeschiedenis van ernstige allergische reacties of bij personen die eerder hebben gereageerd op een hepatitis B-vaccin of een van de componenten ervan, inclusief gist. Herblootstelling kan leiden tot een mogelijk levensbedreigende allergische reactie voor het hele lichaam, bekend als anafylaxie.
Tot op heden zijn er geen studies bij mensen gedaan naar het effect van Heplisav-B tijdens zwangerschap of borstvoeding. Een dierstudie meldde echter geen bijwerkingen bij zwangere laboratoriumratten of hun nakomelingen na een dosis van 0,3 ml Heplisav-B.
Wie moet worden gevaccineerd
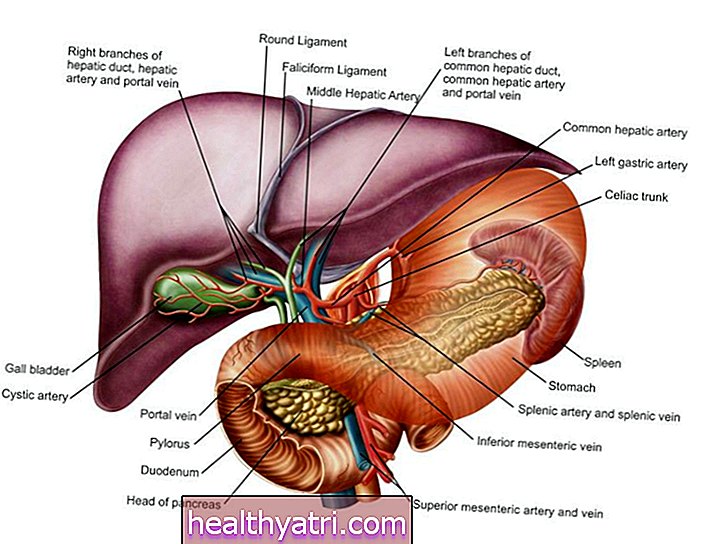
Hepatitis B is een virale ziekte van de lever die chronisch kan worden en kan leiden tot cirrose, leverkanker en overlijden.
Volgens een rapport van de Amerikaanse Preventive Services Task Force (USPSTF), ergens tussen de 700.000 en 2.2. miljoen mensen worden verondersteld besmet te zijn met HBV in de Verenigde Staten. Het aantal infecties is het hoogst bij volwassenen van 30 tot 49 jaar, van wie de meesten besmet raken door onbeschermde seks of door gedeeld gebruik van naalden.
Er is geen remedie voor hepatitis B, maar effectieve vaccinatie kan de ziekte voorkomen. Om deze reden beveelt de Adviescommissie voor immunisatiepraktijken (ACIP) momenteel aan dat alle kinderen hun eerste dosis HBV-vaccin bij de geboorte krijgen en de reeks tussen zes en 18 maanden voltooien. Oudere kinderen en adolescenten die het HBV-vaccin niet hebben gekregen, moeten ook worden gevaccineerd.
De Centers for Disease Control and Preventions beveelt verder aan dat alle volwassenen met een hoog risico op HBV worden gevaccineerd. Waaronder:
- Personen die leven of seks hebben met iemand die hepatitis B heeft
- Seksueel actieve personen die geen langdurige, wederzijds monogame relatie hebben
- Personen die getest of behandeld willen worden voor een seksueel overdraagbare infectie
- Mannen die seks hebben met mannen
- Mensen met hiv
- Mensen die naalden, spuiten of andere drugsparafernalia delen
- Beroepsbeoefenaren in de gezondheidszorg en anderen die risico lopen op blootstelling aan bloed
- Mensen met nierziekte in het eindstadium
- Mensen met een chronische leverziekte
- Mensen met diabetes onder de 60 jaar begonnen zo snel mogelijk na diagnose
- Internationale reizigers naar regio's met matige tot hoge percentages hepatitis B.
- Personen die zijn geëmigreerd uit landen met matige tot hoge percentages hepatitis B of kinderen van ouders die vóór hun geboorte uit deze landen zijn geëmigreerd
- Iedereen die van mening is dat ze gevaar lopen
De USPSTF beveelt momenteel geen HBV-vaccinatie aan voor de algemene volwassen bevolking, aangezien niet is aangetoond dat de praktijk het risico op levergerelateerde ziekte of overlijden vermindert.
Veiligheidsproblemen onderzoeken
Ondanks een overwegend positieve ontvangst door volksgezondheidsfunctionarissen, blijft het vaccin te kampen met veiligheidsproblemen, gezien de vroege afwijzing door de FDA.
De FDA verwierp het vaccin in 2013 aanvankelijk op basis van een van de componenten ervan, bekend als CpG 1018. Dit is de stof die wordt gebruikt om het immuunsysteem van het vaccin te stimuleren en juist degene die de tweeledige serie mogelijk maakt.
Volgens de reactie van de FDA werd aangenomen dat CpG 1018 het potentieel had om bepaalde auto-immuunziekten te veroorzaken, waaronder schildklieraandoeningen. Hoewel de eerste onderzoeken geen statistisch verschil lieten zien tussen Heplisav-B en Engerix-B, werd de aanvraag geweigerd simpelweg omdat de omvang van het onderzoek destijds als te klein werd beschouwd.
Tegen de tijd van het opnieuw aanbrengen waren 14.238 mensen aan het vaccin blootgesteld, met slechts twee gevallen van Hashimoto-thyroïditis (een vorm van schildklieraandoening) en één geval van vitiligo.
Later, in 2016, werd het vaccin ook afgewezen toen een studie een groter dan verwacht aantal hartaandoeningen meldde, waaronder hartaanvallen. In dit geval vroeg de FDA om aanvullende informatie over alle niet-geassocieerde factoren die de resultaten beter zouden kunnen verklaren.
Na beoordeling van de aanvullende gegevens heeft de FDA goedkeuring verleend. De uiteindelijke onderzoeksresultaten rapporteerden een risico van 0,1% op een hartaanval bij mensen die Heplisav-B kregen, versus 0,2% die Engerix-B kregen.












.jpg)