Het nieuwe coronavirus (COVID-19) is uitgegroeid tot een pandemie die wereldwijd miljoenen mensen heeft besmet. Wetenschappers en onderzoekers werken actief aan het vinden van behandelingen voor de ziekte, en idealiter vinden ze een manier om infectie in de eerste plaats te voorkomen.
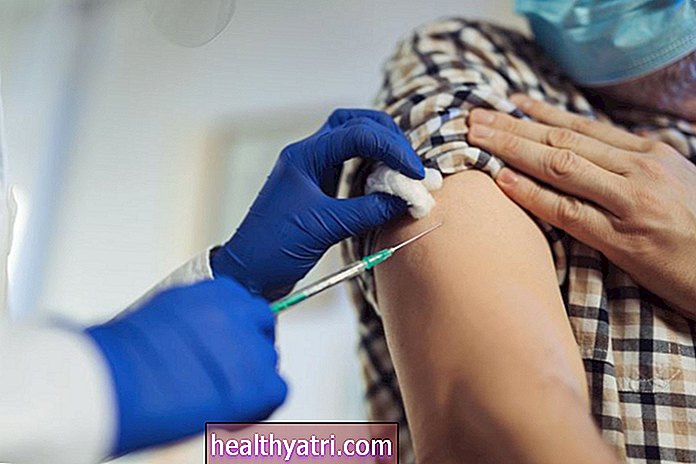
Geber86 / Getty ImagesEr zijn honderden klinische onderzoeken gaande om de potentiële effectiviteit van bestaande medicijnen en nieuwe medicijnen te evalueren en om de levensvatbaarheid van vaccins en bloedproducten te testen. Het volgende schetst een lijst van spraakmakende behandelingen die tegen het virus zijn getest, te beginnen met de behandelingen die momenteel klinisch worden gebruikt tot de behandelingen die nog worden onderzocht.
Sinds december 2020 hebben negen behandelingen toestemming voor gebruik in noodgevallen van de Amerikaanse Food and Drug Administration (FDA), in volgorde van goedkeuring: remdesivir (mei 2020), herstellend plasma (augustus 2020), bamlanivimab monoklonaal antilichaam (november 2020), baricitinib gecombineerd met remdesivir (november 2020), gecombineerde casirivimab en imdevimab monoklonale antilichamen (november 2020), het Pfizer-BioNTech mRNA-vaccin (december 2020), het Moderna mRNA-vaccin (december 2020), gecombineerde bamlanivimab en etesevimab monoklonale antilichamen (februari 2021), en het adenovirusvaccin van Johnson & Johnson (februari 2021).
Remdesivir
Remdesivir is in eerste instantie ontwikkeld als behandeling tegen ebola. Nadat in vitro-onderzoeken hadden aangetoond dat het mogelijk effectief is tegen COVID-19, kregen ziekenhuizen met verzoeken om compassionate use toegang tot het medicijn voor de behandeling van ernstig zieke patiënten. Op 1 mei werd het de eerste behandelingsoptie voor COVID-19 die toestemming voor noodgebruik kreeg van de FDA. De FDA heeft toegestaan dat het wordt gebruikt bij volwassenen en kinderen die in het ziekenhuis zijn opgenomen met ernstige gevallen van de ziekte. Op 22 oktober werd remdesivir het eerste medicijn dat door de FDA werd goedgekeurd om COVID-19 te behandelen zonder toestemming voor gebruik in noodgevallen. Op 19 november werd het ook goedgekeurd voor een nieuwe EUA bij gebruik in combinatie met baricitinib (zie Biologics hieronder).
Wat het onderzoek zegt
Een studie gepubliceerd in deNew England Journal of Medicineonderzocht 61 gevallen van compassionate use van remdesivir-behandeling onder COVID-19-patiënten in het ziekenhuis. Deze patiënten waren ernstig ziek; aan het begin van de studie waren er 30 op mechanische ventilatie en vier op extracorporale membraanoxygenatie (ECMO). Gedurende gemiddeld 18 dagen had 68% van de patiënten verbeterde oxygenatie en 57% van de mensen op beademingsapparatuur kon worden geëxtubeerd. Maar liefst 60% had bijwerkingen en 23% van de mensen (allemaal in de mechanische beademingsgroep) ontwikkelden ernstige complicaties, waaronder meervoudig orgaandisfunctiesyndroom, septische shock, acuut nierletsel en hypotensie.
Een klinische studie - de Adaptive COVID-19 Treatment Trial (ACTT) - door de National Institutes of Health (NIH) - toonde aan dat mensen met ernstige COVID-19-infecties die met het medicijn werden behandeld de symptomen 4 dagen eerder verbeterden (31% sneller) dan degenen die niet werden behandeld. Hoewel er een verbetering leek te zijn in het totale overlevingspercentage, was dit niet statistisch significant. Mensen met matige infecties vertoonden echter geen significante verbetering bij behandeling met 10 dagen remdesivir versus standaardzorg. Hoewel er verbeteringen waren voor mensen die werden behandeld met 5 dagen remdesivir-behandeling, merkten de onderzoekers op dat "het verschil van onzeker klinisch belang was.
Gegevens vrijgegeven door de medicijnfabrikant Gilead Sciences merkten verbeterde klinische resultaten op in een gerandomiseerde controlestudie. Mensen die met COVID-19 in het ziekenhuis waren opgenomen, werden gedurende 10 dagen behandeld met remdesivir (n = 541) of placebo (n = 521). Mensen in de behandelde groep herstelden vijf dagen eerder dan die in de controlegroep, hadden minder dagen zuurstofondersteuning nodig en hadden meer kans om eerder te worden ontslagen.
Daarentegen vond de Wereldgezondheidsorganisatie (WHO) geen klinisch voordeel in hun Solidariteitsproef. Deze studie omvatte bijna 11.300 ziekenhuispersoneel met COVID-19 in 30 landen. Deelnemers aan de studie kregen een van de vier behandelingen: hydroxychloroquine, interferon, lopinavir-ritanovir of remdesivir. Geen van de behandelingen verminderde het sterftecijfer gedurende 28 dagen of de noodzaak om met beademingstherapie te beginnen. Sinds die tijd heeft de WHO formeel het gebruik van het medicijn voor ziekenhuispatiënten afgeraden. Gilead Sciences heeft deze resultaten betwist en er is een collegiale toetsing aan de gang.
De National Institutes of Health beveelt remdesivir, dexamethason of een combinatie van remdesivir met dexamethason aan voor in het ziekenhuis opgenomen COVID-19-patiënten die conventionele zuurstoftherapie nodig hebben.
Dexamethason en methylprednisolon
Dexamethason en methylprednisolon zijn steroïden die vaak worden gebruikt om ontstekingen te behandelen. Ze zijn verkrijgbaar in zowel orale als IV-formuleringen. COVID-19 is in veel gevallen in verband gebracht met een ernstige ontstekingsreactie, en onderzoekers keken naar de voordelen van het gebruik van deze veel voorkomende ontstekingsremmende medicijnen.
Wat het onderzoek zegt
De RECOVERY-studie (Randomized Evaluation of COVid-19 thERapY) -studie) heeft aangetoond dat behandeling met eenmaal daags dexamethason gedurende 10 dagen de klinische resultaten verbeterde in vergelijking met placebo. Specifiek daalde het sterftecijfer van 41% naar 29% voor patiënten die op beademingsapparatuur werden geplaatst en van 26% naar 23% voor mensen die zuurstof nodig hadden zonder beademingstherapie. Patiënten die geen zuurstof- of beademingstherapie nodig hadden, zagen geen klinisch voordeel van dexamethason.
Een meta-analyse, gesponsord door de Wereldgezondheidsorganisatie (WHO), beoordeelde 7 gerandomiseerde klinische onderzoeken met ongeveer 1700 ernstig zieke COVID-19-patiënten. Gepubliceerd inJAMAbleek uit de studie dat het sterftecijfer van 28 dagen significant lager was voor mensen die werden behandeld met steroïden (dexamethason, hydrocortison of methylprednisolon) dan voor degenen die met de gebruikelijke zorg of placebo werden behandeld (32% absolute mortaliteit voor steroïden versus 40% voor controles) .
Steroïden hebben voordelen getoond bij gebruik in combinatie met tocilizumab (zie rubriek Biologie hieronder). Een studie in deAnnalen van de reumatische aandoeningenbeoordeelde patiënten met COVID-19 die ook cytokinestorm hadden, een syndroom van overactieve ontsteking in het lichaam. Patiënten met COVID-19 en Cytokine Storm werden gedurende vijf dagen behandeld met een hoge dosis glucocorticoïde, methylprednisolon. Als ze binnen twee dagen geen klinische verbetering begonnen te krijgen, kregen ze ook een dosis IV tocilizumab. In vergelijking met mensen die met ondersteunende zorg werden behandeld, had de behandelde groep 79% meer kans op klinische verbetering van ademhalingssymptomen gedurende 7 dagen, 65% minder kans op overlijden in het ziekenhuis en 71% minder kans op mechanische beademing. Een andere studie, deze inBorst, bevestigde het voordeel van de bevinding van gecombineerde therapie bij 5776 patiënten die met COVID-19 in het ziekenhuis waren opgenomen. Corticosteroïden verminderden de mortaliteit met 34%, maar de mortaliteit daalde met 56% wanneer ze werden gecombineerd met tocilizumab.
Kinderen die een multisysteemontstekingssyndroom bij kinderen (MIS-C) ontwikkelen, kunnen baat hebben bij methylprednisolon, volgens een onderzoek inJAMAIn de studie werden 111 kinderen met het syndroom behandeld met IV immunoglobuline met of zonder methylprednisolon. Kinderen die beide behandelingen kregen, hadden verbeterde resultaten, met name verminderde koorts binnen 2 dagen en verminderde koortsherhaling gedurende 7 dagen.
Herstellend plasma
Medicijnen zijn een manier om COVID-19 aan te pakken, maar ons eigen lichaam kan ook een manier bieden om de ziekte te bestrijden. Wanneer we worden blootgesteld aan een vreemde stof zoals COVID-19, kan ons immuunsysteem er antilichamen tegen ontwikkelen. Bloed dat deze antilichamen bevat, wordt herstellend plasma genoemd.
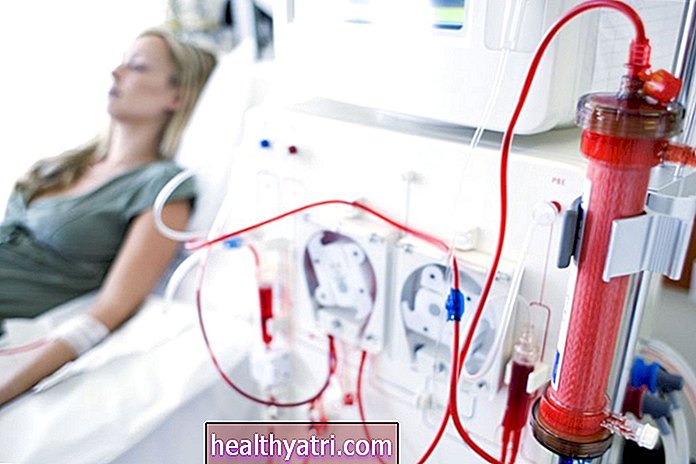
Het verwijderen van bloedplasma van iemand die ziek is en het vervangen door herstellend plasma van iemand die hersteld is van COVID-19, kan hen helpen de infectie te bestrijden. Dit proces staat bekend als plasma-uitwisseling.
Wat het onderzoek zegt
Twee kleine onderzoeken toonden het potentiële voordeel aan van het gebruik van herstellend plasma voor de behandeling van ernstige gevallen van infectie. Een casusreeks omvatte vijf patiënten met ernstige longontsteking die mechanische beademing nodig hadden. Een afzonderlijke pilotstudie omvatte 10 patiënten met ernstige COVID-19-infecties. Alle patiënten ondergingen een transfusie met herstellend plasma. Beide onderzoeken merkten verbeterde symptomen op binnen drie dagen en verminderde virale belasting binnen twee weken (12 dagen voor de casusreeks, zeven dagen voor de pilotstudie). Het vermogen om van een beademingsapparaat af te komen was echter traag en werd niet voor alle patiënten bereikt. Het belangrijkste was dat er geen schade leek te zijn veroorzaakt door de behandeling.
In april 2020 keurde de FDA twee gerandomiseerde, placebogecontroleerde klinische onderzoeken bij Johns Hopkins Medicine goed om te zien of bloedplasma zou kunnen helpen om COVID-19-infectie te voorkomen, niet alleen om ernstig geïnfecteerde personen te behandelen.
De resultaten zijn gevarieerd. Positief is dat een studie inMayo Clinic Proceedingsmerkte op dat niet alleen herstellend plasma over het algemeen veilig was wanneer het werd gebruikt om 20.000 in het ziekenhuis opgenomen COVID-19-patiënten te behandelen, maar dat het in verband kan worden gebracht met een verminderde mortaliteit, vooral wanneer het eerder in de loop van de ziekte wordt toegediend. De grootste studie tot nu toe behandelde meer dan 35.000 ziekenhuispatiënten met herstellend plasma. De bevindingen suggereerden dat behandeling met plasma met hoge antilichaamspiegels de mortaliteit verlaagde indien gegeven binnen 3 dagen na de diagnose. Een onderzoek onder 160 COVID-19-patiënten wees uit dat het behandelen van senioren van 65 jaar en ouder binnen 3 dagen met milde symptomen hun risico op progressie naar ernstige luchtwegaandoeningen met de helft verminderde (16% met behandeling versus 31% met placebo) gedurende 15 dagen. Hoewel de mortaliteit niet in de studie werd beoordeeld, schatten de onderzoekers dat slechts zeven senioren zouden moeten worden behandeld om de ernstige ziekte bij één volwassene te verminderen.
Niet al het onderzoek was even gunstig. Een studie onder bijna 500 volwassenen merkte op dat hoewel herstellend plasma de virale last binnen 7 dagen verminderde, er geen afname van het sterftecijfer was. Een gerandomiseerde gecontroleerde studie met 228 volwassenen met COVID-19-pneumonie vond geen klinisch voordeel voor degenen die gedurende 30 dagen met herstellend plasma werden behandeld. De National Institutes of Health stopten in maart 2021 een klinische proef en merkten op dat er geen voordeel was voor mensen met milde tot matige COVID-symptomen.
Zonder meer consistente of robuuste gegevens is er controverse geweest over de noodtoestemming van de FDA voor herstelplasma als behandeling voor COVID-19 in augustus 2020. In februari 2020 werd de EUA bijgewerkt. Alleen herstellend plasma met een hoge antilichaamtiter is nu goedgekeurd voor gebruik. Het is ook beperkt tot ziekenhuispatiënten in het begin van hun ziekte of tot gehospitaliseerde patiënten die immuungecompromitteerd zijn.
Herstellend plasma kan worden verzameld als een bloeddonatie, en er worden technieken toegepast om te verzekeren dat het plasma vrij is van infectie. Momenteel wordt aanbevolen dat iemand ten minste twee weken symptoomvrij is voordat hij plasma doneert.
Tientallen Amerikaanse ziekenhuizen maken nu deel uit van het National COVID-19 Convalescent Plasma Project en werken samen om therapeutische plasma-uitwisseling te onderzoeken.
Regeneron Pharmaceuticals —Casirivimab en Imdevimab (voorheen REGN-COV2)
Regeneron Pharmaceuticals Inc. ontwikkelde een kunstmatige antibioticacocktail die aanvankelijk REGN-COV2 heette, nu bekend als casirivimab en imdevimab. De onderzoeksbehandeling omvat twee antilichamen die zijn gericht tegen COVID-19. Het bedrijf kondigde voorlopige gegevens aan die erop duiden dat virale ladingen en COVID-19-symptomen binnen 7 dagen na de behandeling waren verminderd. Nadat nog eens 524 mensen aan hun onderzoek waren toegevoegd, bleek REGN-COV2 de behoefte aan COVID-gerelateerde medische bezoeken op dag 29 te verminderen in vergelijking met mensen die werden behandeld met placebo (2,8% versus 6,8%). De proeven werden opgeschort voor mensen die zuurstof met hoge doorstroming of mechanische ventilatie nodig hadden op basis van "een ongunstig risico / batenprofiel" in deze groepen. President Donald Trump, die op 1 oktober positieve COVID-19-testresultaten rapporteerde, werd op 2 oktober 2020 behandeld met REGN-COV2.
Op 21 november verleende de FDA toestemming voor noodgebruik voor de antilichaamcocktail voor mensen met COVID-19 met milde tot matige ziekte die een hoog risico lopen op complicaties, die niet in het ziekenhuis worden opgenomen en die geen aanvullende zuurstof nodig hebben. De National Institutes of Health stelt echter dat deze behandeling geen standaardbehandeling mag zijn, aangezien er "onvoldoende gegevens zijn om het gebruik van casirivimab plus imdevimab voor de behandeling van poliklinische patiënten met milde tot matige COVID-19 aan te bevelen".
Regeneron publiceerde de resultaten van de fase 3-studie in een persbericht, waarin werd aangekondigd dat hun casirivimab-imdevimab-cocktail de COVID-19-infectie verlaagde bij mensen met een hoog risico. In de studie werden 400 mensen gerandomiseerd naar behandeling of placebo. Mensen die de cocktail kregen (n = 186) ontwikkelden geen symptomatische infecties, hoewel 10 asymptomatische infecties ontwikkelden. De placebogroep (n = 223) ontwikkelde echter 8 symptomatische infecties en 23 asymptomatische infecties. Al met al verminderde de behandeling het aantal gevallen van COVID-19-infectie met de helft (5% voor de behandelingsgroep versus 10% voor placebo) en was het volledig beschermd tegen symptomatische infectie.
Andere synthetische antilichamen
Regeneron Pharmaceuticals Inc. is niet het enige bedrijf dat de effectiviteit van synthetische antilichamen die in het laboratorium worden gemaakt, wil onderzoeken.
Eli Lilly - Bamlanivimab
Eli Lilly and Company, gedeeltelijk gesponsord door het National Institute of Allergy and Infectious Diseases, heeft een monoklonaal antilichaam ontwikkeld (aanvankelijk bekend als LY-CoV555, sindsdien bamlanivimab genoemd) bedoeld om COVID-19 te neutraliseren. In klinische fase 2-onderzoeken werden 452 mensen behandeld met elk 3 doses. Hoewel de virale ladingen na de tweede dosis waren afgenomen, hadden de behandelings- en placebogroepen vergelijkbare virale ladingen na de derde dosis. De behandeling verminderde echter de ernst van de symptomen van dag 2 tot en met 6 en verminderde het aantal mensen dat op dag 29 in het ziekenhuis bleef (1,6% versus 6,3%). Het onderzoek vorderde naar klinische fase 3-onderzoeken en een combinatiebehandeling met remdesivir in de ACTIV-3-studie. Op 13 oktober werden echter niet-gespecificeerde bezorgdheid over de veiligheid geuit over de behandeling en werd het proces opgeschort voor in het ziekenhuis opgenomen patiënten.
Op 9 november heeft de FDA een vergunning voor noodgebruik afgegeven voor deze behandeling voor mensen met een hoog risico die milde tot matige COVID-19 hebben, die niet in het ziekenhuis zijn opgenomen en die vanwege hun COVID-19-infectie geen zuurstoftherapie nodig hebben.
In december werd een onderzoek onder 314 mensen met milde tot matige COVID-19 gepubliceerd inNew England Journal of MedicineAlle deelnemers aan de studie werden behandeld met remdesivir en, indien van toepassing, zuurstof en / of dexamethason. Ze werden vervolgens gerandomiseerd om bamlanivimab of placebo te krijgen. De onderzoekers merkten op dat mensen die met het neutraliserende antilichaam waren behandeld, op dag 5 geen verbetering van de ademhalingssymptomen hadden. De studie stopte met rekruteren vanwege een gebrek aan effect.
In een persbericht rapporteerde Eli Lilly de effectiviteit van bamlanivimab als preventieve therapie. In hun BLAZE-2-studie (resultaten nog niet gepubliceerd) werden 965 verpleeghuisbewoners die aanvankelijk negatief testten op COVID-19, behandeld met het monoklonale antilichaam of placebo. Gedurende 8 weken hadden degenen die met bamlanivimab werden behandeld 57% minder kans op het ontwikkelen van symptomatische COVID-19. Vier mensen stierven aan hun infectie, maar geen van hen zat in de behandelingsgroep.
In februari 2020 verleende de FDA een vergunning voor gebruik in noodgevallen voor een combinatie van de monoklonale antilichamen bamlanivimab en etesevimab. De behandeling is bedoeld voor niet-gehospitaliseerde patiënten met milde tot matige COVID-19-symptomen die geen aanvullende zuurstof nodig hebben. Patiënten moeten 12 jaar of ouder zijn, minstens 40 kg wegen en als hoog risico worden beschouwd (bijv. 65 jaar of ouder zijn, bepaalde chronische medische aandoeningen hebben, enz.). Een gerandomiseerde, dubbelblinde, placebogecontroleerde klinische studie onder 1035 mensen wees uit dat degenen die deze behandeling kregen, minder kans hadden om in het ziekenhuis te worden opgenomen of te overlijden aan COVID-19 (2% versus 7%).
In een fase 3-onderzoek werden 769 COVID-19-patiënten behandeld met de combinatie van monoklonale antilichamen of placebo. Alle deelnemers waren 12 jaar of ouder, werden als risicovol beschouwd, hadden milde tot matige symptomen en werden bij aanvang van het onderzoek niet in het ziekenhuis opgenomen. Vier mensen in de behandelde groep moesten uiteindelijk in het ziekenhuis worden opgenomen (4/511), terwijl 15 mensen in de placebogroep in het ziekenhuis werden opgenomen, van wie er 4 overleden (15/258). In totaal verminderde de combinatie van bamlanivimab en etesevimab het risico op ziekenhuisopname of overlijden met 87%.
AstraZeneca - AZD7442
AstraZeneca zal fase 3 klinische onderzoeken starten om uit te vinden of onderzoek naar antilichamen (AZD7442) COVID-19-infectie zou kunnen behandelen en hopelijk kunnen voorkomen. Preklinische studies toonden effectiviteit aan bij muizen, maar het wordt nog niet klinisch gebruikt.
Vaccins voor COVID-19
De beste hoop voor het beheer van COVID-19 op de lange termijn is het ontwikkelen van een vaccin. Vaccins stellen uw lichaam bloot aan een antigeen - een stof die een immuunrespons veroorzaakt, in dit geval van een virus - en zet de productie van antilichamen op gang door uw immuunsysteem. Het doel is om antilichamen tegen het virus te maken zonder een infectie te veroorzaken. Op die manier onthoudt uw lichaam, als u weer aan dat antigeen wordt blootgesteld, hoe het die antilichamen ertegen moet maken. Hopelijk is uw immuunrespons zo sterk dat u helemaal niet ziek wordt. Maar als u toch ziek wordt, zullen uw symptomen milder zijn dan wanneer u het vaccin niet heeft gekregen.
COVID-19-vaccins: blijf op de hoogte van de beschikbare vaccins, wie ze kan krijgen en hoe veilig ze zijn.
Zes belangrijke vaccinkandidaten hebben klinische proeven ondergaan in de Verenigde Staten.
Pfizer Inc. —Vaccin-kandidaat BNT162b2
Werkzaamheid: in november 2020 suggereerden vroege gegevens van een fase III-onderzoek dat een mRNA-vectorvaccin ontwikkeld door Pfizer en BioNTech voor 90% effectief zou kunnen zijn bij het voorkomen van COVID-19. Het vaccin wordt toegediend in een reeks van twee doses, met een tussenpoos van drie weken. Bij het kijken naar de infectiegraad 7 dagen na een tweede dosis, ontwikkelden 94 mensen symptomatische COVID-19 uit een onderzoekspopulatie van 43.538 mensen (30% waren mensen van kleur). Dit bracht hun vaccin op meer dan 90% werkzaamheid. Ze publiceerden 9 dagen later, op 18 november, aanvullende gegevens, waarbij ze opmerkten dat 170 gevallen van symptomatische COVID-19 waren voorgekomen bij proefpersonen, 8 gevallen bij degenen die het vaccin namen en 162 bij mensen die de placebo hadden gebruikt. Dit verbeterde hun gegevens om een algehele werkzaamheid van 95% te laten zien, een werkzaamheid van 94% bij mensen ouder dan 65 jaar. Na het bekijken van die gegevens, bracht de FDA een briefing uit in december waarin werd opgemerkt dat de infectiegraad voor gevaccineerde studiedeelnemers al 10 tot 14 dagen na hun eerste dosis afnam. Massale vaccinatie van bijna 600.000 mensen in Israël heeft resultaten opgeleverd die vergelijkbaar zijn met die in de klinische onderzoeken van Pfizer. Na de tweede dosis bleek 92% effectief te zijn tegen COVID-19 in het algemeen - 94% tegen symptomatische ziekte en 90% tegen asymptomatische ziekte. In een pre-print U.K. case-control-studie werd ook gekeken naar de effectiviteit van vaccinatie in de echte wereld. Als we kijken naar ongeveer 157.000 senioren ouder dan 70 jaar, was een enkele dosis vaccin effectief tegen symptomatische ziekten met percentages van 37% na 14 dagen, 55% na 21 dagen, 61% na 28 dagen en 57% op 35 dagen na een enkele dosis. dosis. Na een tweede dosis nam de effectiviteit toe tot 85 tot 90%. Mensen die symptomatische COVID-19 ontwikkelden na hun eerste dosis, hadden 43% minder kans op ziekenhuisopname binnen 14 dagen na hun diagnose en hadden 51% minder kans om te overlijden aan hun infectie.
Virusvarianten
Sommige stammen van het virus, ook wel varianten genoemd, hebben mutaties in het spike-eiwit ontwikkeld die de effectiviteit van sommige vaccins kunnen veranderen. Tot op heden zijn er veel varianten ontdekt. Hier zijn drie van de meest onderzochte.
- Britse variant: ook bekend als B.1.1.7 of 20I / 501Y.V1, deze variant bevat 17 mutaties (waarvan 8 in het spike-eiwit) en werd voor het eerst gedetecteerd in september 2020.
- Zuid-Afrikaanse variant: ook bekend als B.1.351 of 20H / 501Y.V2, deze variant bevat 21 mutaties (waarvan 10 in het spike-eiwit) en werd voor het eerst gedetecteerd in oktober 2020.
- Braziliaanse variant: ook bekend als B.1.28.1 of 20J / 501Y.V3, deze variant bevat 17 mutaties (waarvan 3 in het spike-eiwit) en werd voor het eerst gedetecteerd in januari 2021.
Virusvarianten: Pfizer beoordeelde het serum van 40 mensen die beide doses van het vaccin met een tussenpoos van 21 dagen hadden gekregen en testte het tegen een virus dat lijkt op het oorspronkelijke virus dat in Wuhan, China werd gedetecteerd (als controle) en vervolgens op een virus met de piek eiwitmutaties gevonden in de Britse variant. Het doel was om te zien hoe effectief het serum was bij het neutraliseren van die virussen. Serum van jongere deelnemers aan het onderzoek (23-55 jaar oud, n = 26) neutraliseerde de Britse variant met 78% en die van oudere deelnemers (57-73 jaar oud, n = 14) met 83%. Vervolgens gingen ze testen tegen andere varianten. Neutraliserende antilichaamassays werden uitgevoerd op het serum van 20 gevaccineerde mensen met behulp van een controlevirus, een virus met de N501Y-mutatie om de Britse en Zuid-Afrikaanse varianten te vertegenwoordigen, 69/70-deletie + N501Y + D614G-mutaties om de Britse variant te vertegenwoordigen, en een virus met E484K + N501Y + D614G-mutaties om de Zuid-Afrikaanse variant te vertegenwoordigen. In 6 van de sera waren titers slechts half zo effectief tegen de Zuid-Afrikaanse variant. Dat gezegd hebbende, in 10 van de sera waren de titers twee keer zo hoog ten opzichte van de Britse variant. Al met al bleef het vaccin effectief tegen deze varianten met een verschil van 0,81 tot 1,46 maal vergeleken met de controle. Een voorlopig rapport van serum van 15 gevaccineerde ontvangers inNew England Journal of Medicinevond een tweederde verminderd vermogen om de B.1.351-variant te neutraliseren. Pfizer onderzoekt een derde vaccindosis als een manier om de antilichaamrespons tegen COVID-19-varianten te versterken.
Kinderen: Pfizer onderzoekt de effectiviteit van hun vaccin bij kinderen. Hun fase III-studie omvat momenteel meer dan 2.200 kinderen van 12 tot 15 jaar en meer dan 750 adolescenten van 16 tot 17 jaar.
Opslag: Er is bezorgdheid geuit over de noodzaak om het vaccin op te slaan met behulp van koelketentechnologie, d.w.z. het te bevriezen bij -70 graden Celsius (-94 graden Fahrenheit). Pfizer ontwikkelde speciale temperatuurgecontroleerde containers met behulp van droogijs met thermische GPS-tracking om te verzekeren dat het vaccin tijdens verzending op de juiste temperatuur werd gehouden. Gegevens die aan de FDA zijn verstrekt, hebben sindsdien aangetoond dat het vaccin tot 2 weken stabiel blijft bij standaard vriestemperaturen. Hierdoor wordt het vaccin hopelijk op meer locaties toegankelijk.
Goedkeuring: Het vaccin werd op 2 december goedgekeurd voor gebruik in het Verenigd Koninkrijk. Op 8 december was de 90-jarige Margaret Keenan uit het Verenigd Koninkrijk de eerste niet-onderzoeksdeelnemer ter wereld die het vaccin ontving. Op 11 december verleende de FDA toestemming voor gebruik in noodgevallen in de Verenigde Staten en op 14 december werden de eerste Amerikanen gevaccineerd.
Controverse: met de toenemende verspreiding van COVID-19, kondigde het Verenigd Koninkrijk plannen aan om vaccindoses met een tussenpoos van 12 weken toe te dienen in plaats van de aanbevolen 3 weken. Hoewel hierdoor het aantal mensen dat een eerste dosis van het vaccin krijgt, zou toenemen, hebben Pfizer en BioNTech verklaard dat hun klinische onderzoeken niet over de gegevens beschikken om de effectiviteit van een dergelijk doseringsschema te ondersteunen. Op dit moment zullen de Verenigde Staten doorgaan met het aanbevolen doseringsschema van drie weken.
Moderna Inc. - Kandidaat-vaccin mRNA-1273
Voorlopige resultaten: Moderna, gefinancierd door het National Institute of Allergy and Infectious Diseases (NIAID) en de Biomedical Advanced Research and Development Authority (BARDA), publiceerde voorlopige resultaten van haar Fase I-vaccinonderzoek in deNew England Journal of Medicinein juli 2020. Na twee doses van het mRNA-vaccin, toegediend met een tussenpoos van vier weken, ontwikkelden de 45 deelnemers aan de studie neutraliserende antilichamen in concentraties die vergelijkbaar zijn met die in herstellend plasma. Een volgende fase II-studie liet veelbelovende resultaten zien bij apen. Vierentwintig resusaapjes werden behandeld met vaccin of placebo en kregen twee injecties met een tussenpoos van vier weken. Ze werden vervolgens direct blootgesteld aan hoge doses COVID-19. Na 2 dagen had slechts 1 op 8 van de gevaccineerde apen een detecteerbaar virus, terwijl alle apen die met placebo werden behandeld de infectie hadden. Nogmaals, de neutraliserende activiteit was significant hoger dan die waargenomen met herstellend serum. Ze ontdekten ook een CD4-T-celrespons tegen het spike-eiwit.
Werkzaamheid: in november 2020 toonden gegevens van hun fase III-onderzoek aan dat het Moderna-vaccin 94,5% was ten opzichte van COVID-10. Als we kijken naar de infectiegraad 2 weken na een tweede dosis, ontwikkelden 95 mensen symptomatische COVID-19 uit een onderzoekspopulatie van meer dan 30.000 mensen, waaronder meer dan 7.000 mensen ouder dan 65 jaar en meer dan 11.000 mensen met een kleur.Maar liefst 42% van de bevolking had aandoeningen met een hoog risico, zoals diabetes, hartaandoeningen of obesitas. Van degenen die de ziekte opliepen, werden 11 gevallen als ernstig vermeld, maar geen van hen had het vaccin gekregen. In december publiceerden ze aanvullende gegevens, waarbij ze opmerkten dat 196 gevallen van symptomatische infectie waren voorgekomen bij proefpersonen, 11 gevallen bij degenen die het vaccin namen (geen enkele had ernstige COVID-19) en 185 bij mensen die de placebo gebruikten. Dit suggereerde 94,1% werkzaamheid voor COVID-19 in het algemeen en 100% werkzaamheid tegen ernstige ziekte. Peer review van de gegevens is in afwachting.
Virusvarianten: Moderna voerde een in vitro-analyse uit en testte het serum van 8 gevaccineerde mensen uit hun fase 1-studie tegen de varianten B.1.1.7 en B.1.351. Het bedrijf beweert dat er geen significante afname was in neutraliserende titers tegen de Britse variant, maar constateerde een 6-voudige afname in titers ten opzichte van de Zuid-Afrikaanse variant. Om deze reden onderzoeken en ontwikkelen ze een boosterdosis die gericht is op de B.1.351-variant. Een voorlopig rapport van serum van gevaccineerde ontvangers in deNew England Journal of Medicinevond een marginale 1,2-voudige afname in het vermogen om de B.1.17-variant te neutraliseren, maar een 6,4-voudige afname ten opzichte van de B.1.351-variant.
Kinderen: Moderna gaat door met beproevingen voor kinderen vanaf 12 jaar.
Immuniteitsduur: Belangrijk is dat Moderna ook gegevens heeft gepubliceerd over de verwachte duur van de vaccinrespons. In een fase I-onderzoek werden 34 mensen beoordeeld die 2 doses van het vaccin kregen met een tussenpoos van 28 dagen en werd hun antilichaamrespons vergeleken met 41 controles die herstelden van COVID-19. De onderzoekers ontdekten dat neutraliserende antilichamen 90 dagen na de tweede dosis vaccin aanhielden en in hogere concentraties dan degenen die de ziekte hadden. Dit biedt hoop dat het vaccin een redelijke periode van immuniteit kan bieden. Er zijn meer langetermijngegevens nodig om de werkelijke duur van de immuunrespons te bepalen.
Opslag: In tegenstelling tot het Pfizer-vaccin, waarvoor koelketentechnologie vereist is, kan het Moderna-vaccin gedurende zes maanden in standaard diepvriezers bij -4 graden Celsius (-20 graden Fahrenheit), 30 dagen bij normale koelkasttemperaturen en 12 uur op kamertemperatuur worden bewaard.
Goedkeuring: De FDA verleende op 18 december 2020 de vergunning voor noodgebruik van Moderna-vaccin. De eerste doses werden toegediend op 21 december. Het VK keurde dit vaccin goed voor gebruik op 8 januari 2021.
Controverse: de FDA overweegt de dosis van het Moderna-vaccin te verlagen om het beschikbare aanbod en het aantal mensen dat met een eerste dosis kan worden gevaccineerd, te vergroten. Gegevens uit fase II-onderzoeken tonen aan dat halve doses van het vaccin hetzelfde immuniteitsniveau boden als volledige doses voor mensen tot 55 jaar oud. Die gegevens omvatten echter honderden mensen en zijn afkomstig van onderzoeken die bedoeld waren om te bepalen of er een immuunrespons op het vaccin was, d.w.z. of er zich antilichamen ontwikkelden. De fase III-onderzoeken waren degenen die de effectiviteit tegen COVID-19 daadwerkelijk beoordeelden. In laatstgenoemde onderzoeken werd de volledige vaccindosis gebruikt.
AstraZeneca - Kandidaat vaccin AZD1222 (voorheen ChAdOx1)
Voorlopige resultaten: in samenwerking met AstraZeneca heeft het Jenner Institute van de Universiteit van Oxford een enorme vlucht genomen op het gebied van vaccinonderzoek. Omdat het vaccin voor een ander type coronavirus vorig jaar veelbelovend was in kleinere proeven bij mensen, kon het Jenner Institute snel vooruitgang boeken. Na een eerste injectie van hun adenovirus-vectorvaccin ontwikkelden zich neutraliserende antilichamen bij 91% van de 35 studiedeelnemers die het vaccin kregen, piekten na 28 dagen en bleven gedurende 56 dagen hoog. Met een boostervaccin na 4 weken werden bij alle deelnemers neutraliserende antilichamen gevonden. Hun vaccin had ook een T-celrespons die na 7 dagen werd opgemerkt, met een piek van 14 dagen en tot 56 dagen aanhield. Het vaccin tijdelijkstopte de fase III-studie in september 2020 nadat een deelnemer transversale myelitis ontwikkelde, een neurologische aandoening die kan worden veroorzaakt door virussen. Nadat werd vastgesteld dat de ziekte niet verband hield met het vaccin, hervatte AstraZeneca de proef na zes weken. In november werden meer peer-reviewed Fase II / III-gegevens gepubliceerd. Met een toename tot 560 deelnemers aan de studie, ontwikkelde 99% van de mensen neutraliserende antilichamen binnen 2 weken na de boosterdosis.
Werkzaamheid: In december publiceerde AstraZeneca door vakgenoten beoordeelde gegevens van meer dan 11.000 deelnemers aan de studie in twee verschillende studies. Het werkzaamheidspercentage van het vaccin was 62% nadat twee vaccins met een volledige dosis een maand na elkaar waren toegediend (n = 8895) en 90% wanneer een halve dosis werd gegeven, gevolgd door een volledige dosis een maand later (n = 2741), voor een gecombineerd werkzaamheidspercentage van 70,4%. In februari hebben ze meer Fase III-gegevens vrijgegeven, dit keer gegevens over een grotere populatie van meer dan 17.100 deelnemers. De werkzaamheid na een enkele dosis was 76% na 22 tot 90 dagen (59% voor de volledige dosisgroep, 86% voor de halve dosisgroep). De werkzaamheid 14 dagen na een regime van twee doses was 67% tegen symptomatische COVID-19 (57% voor de volledige dosisgroep, 74% voor de halve dosisgroep). Interessant genoeg werd de werkzaamheid ook beïnvloed door de timing van de doses. Het was zo laag als 55% wanneer de doses werden toegediend met een tussenpoos van minder dan 6 weken (33% voor de volledige dosisgroep, 67% voor de halve dosisgroep), maar steeg tot 82% wanneer de doses werden gescheiden door ten minste 12 weken (63 % voor de volledige dosisgroep, 92% voor de halve dosisgroep). Merk op dat deze werkzaamheid is gebaseerd op het feit dat iemand symptomen van COVID-19 ontwikkelt en geen weerspiegeling is van asymptomatische COVID-19-infectie. In een preprint case-control-studie uit het Verenigd Koninkrijk werd gekeken naar de effectiviteit van vaccinatie met een enkelvoudige dosis bij mensen ouder dan 70 jaar. De onderzoekers keken naar ongeveer 157.000 mensen die in de echte wereld op COVID-19 werden getest. De effectiviteit van het vaccin tegen symptomatische ziekte was 22% na 14 dagen, 45% na 21 dagen, 60% na 28 dagen en 73% na 35 dagen. Mensen die ondanks vaccinatie symptomatische COVID-19 ontwikkelden, hadden 37% minder kans op ziekenhuisopname binnen 14 dagen na hun diagnose.
Virusvarianten: om de werkzaamheid tegen de B.1.1.7-variant te controleren, hebben onderzoekers de sequentie bepaald van het virale genoom van 499 Fase II / III-deelnemers die COVID-19 hadden gecontracteerd. Er was een 9-voudige afname van neutraliserende antilichamen tegen B.1.1.7 in vergelijking met het oorspronkelijke virus. Voor mensen die aan de B.1.1.7-variant waren blootgesteld, was de werkzaamheid 75% tegen symptomatische COVID-19-infectie, maar slechts 27% tegen asymptomatische infectie. Dit was in tegenstelling tot respectievelijk 84% en 75% voor de oorspronkelijke stam. Helaas werd de toediening van vaccins in Zuid-Afrika stopgezet nadat uit gegevens bleek dat het niet effectief was tegen milde tot matige COVID-19 veroorzaakt door B.1.351.
Opslag: In tegenstelling tot de mRNA-vaccins hoeft het vaccin niet te worden ingevroren en kan het worden bewaard bij normale gekoelde temperaturen.
Goedkeuring: Het vaccin werd op 30 december 2020 goedgekeurd voor gebruik in het Verenigd Koninkrijk. De eerste doses werden toegediend op 4 januari 2021. De Wereldgezondheidsorganisatie adviseerde het gebruik van het vaccin in februari 2020.
Controverse: vergelijkbaar met het Pfizer-vaccin heeft het Verenigd Koninkrijk een wijziging aangekondigd in het doseringsschema van het AstraZeneca-vaccin van 4 weken naar 12 weken tussen de doses. Beschikbare gegevens suggereren dat er een vergelijkbare werkzaamheid is bij toediening met deze frequentie voor mensen die de volledige dosis van het vaccin hebben gekregen.
Johnson & Johnson - Kandidaat vaccin Ad26.COV2.S
Voorlopige resultaten: Dit vaccin wordt ontwikkeld door Janssen Pharmaceutical Companies, een divisie van Johnson en Johnson. Het is een vaccin met adenovirusvectoren dat het spike-eiwit aanvalt dat tot expressie wordt gebracht door SARS-CoV-2. Een onderzoek bij 52 resusaapapen wees uit dat een enkele injectie een neutraliserende antilichaamrespons opwekte met bescherming tegen het virus. Een fase I / II-studie met 56 volwassenen beoordeeld op veiligheid met een schema met een enkele dosis of twee doses. Na één dosis was de seroconversie (ontwikkeling van antilichamen tegen het spike-eiwit) 99% en de T-celrespons tegen het spike-eiwit bereikte 83%. Het vaccin is veelbelovend omdat het de enige huidige kandidaat is waarvoor een enkele dosis nodig is in plaats van twee doses in serie. In oktober 2020 meldde Johnson & Johnson een onverklaarbare ziekte bij een van hun studiedeelnemers. Het bedrijf stopte hun klinische proef 11 dagen totdat zeker was dat de ziekte geen verband hield met het vaccin. Sindsdien zijn er meer Fase I / II-gegevens gepubliceerd, die een neutraliserende antilichaamrespons laten zien in twee verschillende leeftijdsgroepen, van 18 tot 55 jaar en van 65 jaar en ouder. Ze vergeleken ook verschillende doseringsregimes, bijvoorbeeld hoge dosis versus lage dosis en enkele dosis versus twee doses met een tussenpoos van 56 dagen. In totaal werden 805 deelnemers gevaccineerd. Op dag 29 had gemiddeld 90% van de mensen neutraliserende antilichamen (92-99% voor het jongere cohort, 88-96% voor het oudere cohort, afhankelijk van het doseringsregime). Op dag 57 was de seroconversie 100% voor iedereen, ongeacht leeftijd of doseringsregime.
Werkzaamheid: hun fase 3-onderzoek omvatte meer dan 43.000 mensen en er waren 468 gevallen van symptomatische COVID-19. Het vaccin was het meest effectief tegen ernstige infecties, met een werkzaamheid van 85% na 28 dagen zonder dat er gevallen werden gedetecteerd na dag 49. De algehele effectiviteit was 66% (72% in de Verenigde Staten, 66% in Latijns-Amerika en 57% in Zuid-Afrika. ). Merk op dat 95% van de gevallen in Zuid-Afrika afkomstig was van de B.1.351-variant.
Goedkeuring: Het Johnson & Johnson-vaccin kreeg op 27 februari 2021 toestemming van de FDA voor noodgebruik als een vaccin met één dosis. De WHO verleende op 12 maart 2021 toestemming.
Novavax Inc. - Kandidaat voor vaccin NVX-CoV2373
Voorlopige resultaten: gesponsord door het National Institute of Allergy and Infectious Diseases (NIAID) en de Biomedical Advanced Research and Development Authority (BARDA), gebruikt dit vaccin nanodeeltjestechnologie om een antilichaamrespons tegen het spike-eiwit te ontwikkelen. Net als veel van de andere vaccins, wordt het in twee doses toegediend met een tussenpoos van 21 dagen. Fase I / II klinische onderzoeken hebben een antilichaamrespons aangetoond die groter is dan die waargenomen in herstellend plasma van patiënten die symptomatisch waren met COVID-19. Er wordt actief ingeschreven voor een fase III-studie met als doel 30.000 deelnemers aan de studie, van wie tweederde het vaccin zal krijgen, de rest een placebo.
Werkzaamheid: in een persbericht maakte het bedrijf de voorlopige resultaten bekend van hun fase 3-studie in het VK (meer dan 15.000 deelnemers) en hun fase 2-studie in Zuid-Afrika (meer dan 4.400 deelnemers). In de vorige studie ontwikkelden 62 deelnemers symptomatische COVID-19 (6 in de behandelde groep versus 56 in de placebogroep). Over het algemeen was de effectiviteit van het vaccin 89,3%. Dit viel terug tot 95,6% ten opzichte van de oorspronkelijke stam en 85,6% ten opzichte van de Britse variant. De laatste studie was minder succesvol en constateerde 44 gevallen van symptomatische COVID-19 (15 in de behandelingsgroep versus 29 gevallen in de placebogroep) met een totale effectiviteit van 60%. De sequentiebepaling werd alleen gedaan bij 27 van de positieve gevallen, maar van 25 daarvan werd bevestigd dat het de Zuid-Afrikaanse variant was.
INOVIO Pharmaceuticals Inc. - Kandidaat voor vaccin INO-4800
De Coalition for Epidemic Preparedness Innovations en The Bill and Melinda Gates Foundation behoren tot de vele financieringsbronnen voor deze vaccinkandidaat. De eerste injecties van dit DNA-vaccin, ontwikkeld door INOVIO Pharmaceuticals, Inc., werden op 6 april 2020 toegediend aan gezonde proefpersonen. In september 2020 zette de FDA klinische fase II / III-onderzoeken uit omdat het de veiligheid van het toedieningshulpmiddel evalueert. injecteert DNA in cellen. Het bedrijf verwacht de proeven in het tweede kwartaal van 2021 te hervatten.
Biologics
Ernstige gevallen van COVID-19 zijn in verband gebracht met een zogenaamde cytokinestorm. Als onderdeel van de normale immuunrespons rekruteert het lichaam cytokinen - eiwitten die worden uitgescheiden door cellen van het immuunsysteem - naar de plaats van infectie. In sommige gevallen wordt dat proces echter hyperreactief en worden overtollige cytokines vrijgegeven. Sommige van deze cytokinen zijn inflammatoir van aard en kunnen leiden tot verergering van ademhalingssymptomen of orgaanfalen. Biologische middelen - farmaceutische behandelingen gemaakt van biologische bronnen - worden nu overwogen om dit aan te pakken.
Baricitinib
Baricitinib is een JAK1 / JAK2-remmer, een klasse medicijnen die worden gebruikt om ontstekingen te bestrijden door het effect van bepaalde cytokines te verminderen.
Wat het onderzoek zegt: als onderdeel van de Adaptive COVID-19 Treatment Trial (ACTT-2), heeft een fase III gerandomiseerde dubbelblinde placebo-gecontroleerde studie een vroege belofte voor het medicijn aangetoond. Ongeveer 1.000 patiënten die met COVID-19 in het ziekenhuis waren opgenomen, werden gerandomiseerd om remdesivir alleen of remdesivir met baricitinib te krijgen. Patiënten verbeterden gemiddeld een dag eerder klinisch met de combinatiebehandeling. In november 2020 keurde de FDA de geneesmiddelencombinatie (niet alleen baricitinib) goed voor een vergunning voor gebruik in noodgevallen voor de behandeling van gehospitaliseerde patiënten die zuurstofsuppletie, beademing of extracorporale membraanoxygenatie (ECMO) nodig hadden. De National Institutes of Health hebben echter verklaard dat er onvoldoende bewijs is om dit regime als voorkeursbehandeling te ondersteunen wanneer dexamethason beschikbaar is.
Interferon Beta-1a
Interferonen zijn een natuurlijk onderdeel van uw immuunsysteem. Deze cytokines versterken de immuunrespons op virussen. Momenteel zijn interferonen momenteel een geïnjecteerde behandeling die wordt gebruikt voor virale hepatitis.
Wat het onderzoek zegt: aangezien COVID-19 in de meeste gevallen een longaandoening is, keken onderzoekers of het inademen van interferon bèta-1a in de longen zou kunnen helpen om de immuunrespons tegen het virus te versterken. Een fase 2 gerandomiseerde dubbelblinde klinische studie inThe Lancet Respiratory Medicinekeek naar ongeveer 100 volwassenen die met COVID-19 in het ziekenhuis waren opgenomen. Deelnemers werden gedurende 14 dagen behandeld met geïnhaleerd interferon bèta-1a via vernevelaar of placebo. De interferongroep had tweemaal de klinische verbetering na 15 tot 16 dagen en driemaal de verbetering op dag 28. Hoewel de duur van een ziekenhuisopname niet afnam, was er een afname van 79% in de ernst van de ziekte of overlijden.
Tocilizumab
Tocilizumab is een monoklonaal antilichaam dat de binding van celreceptoren aan interleukine-6 (IL-6), een van de pro-inflammatoire cytokines, blokkeert. Dit zou in theorie helpen om de ernst van de cytokinestorm te verminderen en mensen te helpen sneller te herstellen.
Wat het onderzoek zegt:
Een studie inLancet Reumatologievond 39% verminderd risico op beademing of overlijden bij COVID-19-pneumoniepatiënten die werden behandeld met tocilizumab in vergelijking met degenen die werden behandeld met standaardtherapie. Tocilizumab werkt echter als een immunosuppressivum en de onderzoekers ontdekten ook dat degenen die met het medicijn werden behandeld, ook een drievoudige toename hadden in het ontwikkelen van andere nieuwe infecties zoals invasieve aspergillose. Volgens een studie van 154 patiënten inKlinische infectieziektenverminderde tocilizumab het sterftecijfer bij COVID-19-patiënten die een beademingsapparaat nodig hadden met 45% in vergelijking met degenen die niet met het geneesmiddel werden behandeld. Hoewel degenen die met tociluzumab werden behandeld, meer kans hadden op het ontwikkelen van superinfecties (54% vs. 26%) gedurende een follow-up van 47 dagen, hadden ze geen verhoogd sterftecijfer als gevolg van die superinfecties.
Er zijn drie onderzoeken gepubliceerd inJAMA Interne geneeskundein oktober 2020, maar de resultaten waren inconsistent. Een Amerikaanse studie behandelde 433 mensen met ernstige COVID-19 binnen twee dagen na hun opname op een intensive care-afdeling. Hun sterftecijfer was 29% vergeleken met 41% voor IC-patiënten die geen tocilizumab kregen. Franse en Italiaanse studies vonden echter geen klinisch voordeel in hun gerandomiseerde open-label studies voor mensen met COVID-19-pneumonie. De eerste studie keek naar 130 mensen met een matige tot ernstige ziekte en de laatste naar 126 mensen. Ze vonden respectievelijk geen verschil in het sterftecijfer na 28 dagen of verbetering van de symptomen met behandeling na 14 dagen. Een andere studie inNew England Journal of Medicinekeek naar bijna 400 mensen die COVID-19-pneumonie hadden. Degenen die met tocilizumab werden behandeld, hadden op dag 28 minder vaak mechanische beademing nodig (12% versus 19% in vergelijking met standaardzorg). Hoewel de klinische resultaten waren verbeterd, veranderden de sterftecijfers niet significant.
Helaas hebben niet alle onderzoeken een voordeel aangetoond. Sommigen hebben potentiële schade getoond. Een Braziliaanse studie onder 129 ernstig zieke COVID-19-patiënten werden behandeld met tocilizumab met standaardzorg of alleen standaardzorg. Na 15 dagen was de mortaliteit zelfs hoger voor degenen die met tocilizumab werden behandeld, 17% versus 3%. Na 29 dagen waren de sterftecijfers niet statistisch significant tussen de twee groepen. Hoewel andere onderzoeken een overlevingsvoordeel hebben aangetoond, werpt dit onderzoek aanzienlijke veiligheidsproblemen op. Om die reden is deze studie zelfs voortijdig beëindigd.
De National Institutes of Health beveelt momenteel tocilizumab plus dexamethason aan voor COVID-19-patiënten op de ICU die mechanische ventilatie of high-flow zuurstof in de neuscanule nodig hebben. Niet-ICU-patiënten die hypoxie ontwikkelen en niet-invasieve beademing of zuurstof met hoge doorstroming nodig hebben, kunnen ook voor dit regime in aanmerking komen, als ze ook verhoogde inflammatoire markers hebben. Dat gezegd hebbende, mag tocilizumab niet worden gebruikt voor mensen die aanzienlijk immuungecompromitteerd zijn.
Andere antivirale middelen
Er zijn momenteel een aantal antivirale behandelingen - medicijnen die voorkomen dat een virus zich kan voortplanten - die momenteel worden onderzocht op COVID-19.
Molnupiravir
Molnupiravir is een medicijn dat de replicatie van sommige RNA-virussen blokkeert. Het is een pro-drug, een inactief medicijn, dat in het lichaam wordt gemetaboliseerd tot zijn actieve vorm (N4-hydroxycytidine). Het medicijn is ontwikkeld door Merck en Ridgeback Biotherapeutics.
Wat het onderzoek zegt: een fase 2 klinische studie omvatte 78 niet-gehospitaliseerde mensen met symptomatische COVID-19 en detecteerbare niveaus van virus op hun nasofaryngeale uitstrijkje. Behandeling met molnupiravir verminderde hun virale last tot 0 op dag 5 (0/47), maar virus bleef detecteerbaar in 24% van de placebogroep (6/25). Aan de behandeling werden geen ernstige bijwerkingen toegeschreven.
Influenza-medicatie
Favipiravir en arbidol zijn antivirale medicijnen die worden gebruikt om griep te behandelen. In hoge concentraties kunnen ze effectief zijn tegen COVID-19.
Wat het onderzoek zegt: in een onderzoek onder 240 COVID-19-patiënten vergeleken onderzoekers de effectiviteit van favipiravir met arbidol. Symptomen van hoesten en koorts verbeterden veel sneller met favipiravir dan met arbidol, maar er was geen significant verschil in het herstelpercentage op dag zeven. Beide medicijnen werden goed verdragen met slechts milde bijwerkingen.
Lopinavir-Ritonavir
Lopinavir-ritonavir is een paar antivirale geneesmiddelen die worden gebruikt om hiv te behandelen en die mogelijk effectief zijn tegen COVID-19.
Wat het onderzoek zegt: In een onderzoek onder 199 mensen met longontsteking door COVID-19 en een laag zuurstofgehalte kregen 94 mensen lopinavir-ritonavir en de rest een placebo. Hoewel meer mensen die met lopinavir-ritonavir werden behandeld de symptomen op dag 14 hadden verbeterd (45,5% vs. 30%), was er geen significant verschil tussen de twee groepen wat betreft de duur van zuurstoftherapie, de behoefte aan mechanische beademing, de duur van ziekenhuisopname of sterftecijfer. In een andere studie werden 127 in het ziekenhuis opgenomen volwassenen met COVID-19 gerandomiseerd naar ofwel drievoudige therapie met lopinavir-ritonavir, ribavirine en interferon β-1b ofwel naar lopinavir-ritonavir alleen. Patiënten in de drievoudige therapiegroep stopten eerder met virusuitscheiding (7 dagen versus 12 dagen), hadden eerder verbetering van de symptomen (4 dagen versus 8 dagen) en verlieten het ziekenhuis eerder (9 dagen versus 15 dagen).
Hydroxychloroquine en Chloroquine
Hydroxychloroquine en chloroquine zijn medicijnen die momenteel door de FDA zijn goedgekeurd voor de behandeling van malaria en auto-immuunziekten zoals lupus en reumatoïde artritis.Door te interfereren met eiwitglycosylatie en andere enzymatische processen, wordt aangenomen dat deze medicijnen kunnen voorkomen dat COVID-19 zich bindt aan, binnendringt in en repliceert in menselijke cellen.
Een studie waarin hydroxychloroquine werd vergeleken met chloroquine, toonde aan dat hydroxychloroquine iets minder krachtig is, maar nog steeds potentieel effectief tegen COVID-19 in vitro.
Wat het onderzoek zegt
Een Franse studie liep voorop in het onderzoek naar hydroxychloroquine en chloroquine. Het omvatte aanvankelijk 26 COVID-19-patiënten die werden behandeld met een hydroxychloroquine-regime en 16 onbehandelde controlepatiënten. Zes van de patiënten die met hydroxychloroquine werden behandeld, werden ook behandeld met azithromycine (ook bekend als een Z-Pack, dat wordt voorgeschreven voor verschillende infecties). Op papier zagen de resultaten er veelbelovend uit. Op dag zes merkten de auteurs van het onderzoek op dat mensen die met hydroxychloroquine werden behandeld, hun virale lading - de hoeveelheid virus in hun bloed - met 57% verminderden, en dat degenen die ook met azitromycine waren behandeld, het virus helemaal hadden geklaard.
Hoewel dit bemoedigend was, ging het onderzoek niet in op hoe het de patiënten klinisch verging, wat betekent of hun symptomen al dan niet beter begonnen te worden. Het was ook onduidelijk of de behandeling leidde tot de medische problemen die de deelnemers aan de studie beletten de onderzoekers op te volgen (één stierf, drie overgebracht naar de intensive care, één stopte de behandeling vanwege bijwerkingen van medicatie, één verliet het ziekenhuis).
Terwijl de FDA in maart, op 15 juni, toestemming voor gebruik in noodgevallen verleende voor zowel chloroquinefosfaat- als hydroxychloroquinesulfaatproducten voor COVID-19, trok zij de autorisatie in, daarbij verwijzend naar ondoelmatigheid en ernstige bijwerkingen.
Hoewel er anekdotisch bewijs is om het gebruik van deze medicijnen te ondersteunen, hebben latere onderzoeken niet dezelfde voordelen aangetoond. Een tweede Franse studie volgde hetzelfde protocol als de oorspronkelijke studie, maar ontdekte dat hydroxychloroquine de symptomen niet significant verbeterde of de klaring van het virus uit het lichaam verminderde. Meerdere andere onderzoeken hebben aangetoond dat hydroxychloroquine niet werkzamer is dan placebo bij de behandeling van mensen die COVID-19 hadden. In september 2020 kwam een dubbelblinde, placebo-gecontroleerde gerandomiseerde klinische studie binnenJAMA Interne geneeskundeconcludeerde dat hydroxychloroquine niet effectief was in het voorkomen van infectie bij 132 gezondheidswerkers. Hetzelfde geldt voor mensen die regelmatig hydroxychloroquine gebruiken om reumatologische aandoeningen te behandelen. Een andere studie toonde aan dat het nemen van hydroxychloroquine hun risico op het oplopen van COVID-19 niet verlaagde in vergelijking met mensen die het medicijn niet gebruikten.
Meer zorgwekkend zijn de mogelijke bijwerkingen van deze medicijnen. Een Braziliaanse studie moest vroegtijdig worden stopgezet vanwege complicaties door hoge doses chloroquine. EENJAMAstudie toonde aan dat behandeling met hydroxychloroquine het QT-interval verlengde bij meer dan 20% van de COVID-19-patiënten, een bevinding op een elektrocardiogram (ECG) die kan worden geassocieerd met de ontwikkeling van levensbedreigende hartritmestoornissen.
Niet alle rapporten zijn slecht. Er is een studie gepubliceerd die potentiële voordelen voor hydroxychloroquine bij de behandeling van COVID-19 laat zien. Onderzoekers bestudeerden meer dan 2500 volwassenen en ontdekten dat mensen die met het medicijn werden behandeld een mortaliteit hadden van 14% vergeleken met 26% zonder het. Wanneer hydroxychloroquine werd gecombineerd met azithromycine, was de mortaliteit 20%. Er is echter controverse over de studie, omdat het aantal mensen dat met het steroïde dexamethason werd behandeld aanzienlijk hoger was in de behandelingsgroepen, wat suggereert dat het voordeel kan voortkomen uit het steroïde in plaats van aan hydroxychloroquine of azithromycine. Terwijl 68% van alle deelnemers aan de studie werd behandeld met steroïden, kreeg slechts 35% in de niet-behandelde groep dexamethason. Ongeveer 79% in de hydroxychloroquine-groep en 74% in de gecombineerde hydroxychloroquine met azithromycinegroep had ook steroïden gekregen.
Een woord van Verywell
Het is belangrijk om hoop te bieden in deze tijd van onzekerheid, maar het is ook noodzakelijk dat we objectieve, wetenschappelijk bewezen manieren vinden om onszelf te beschermen. Met honderden klinische onderzoeken in de maak, moeten we waakzaam blijven als het gaat om het onderzoeken van wat werkt en wat niet. Behandelingen moeten bewezen veilig en effectief zijn voordat we ze gebruiken om grote delen van de bevolking te behandelen.



















-is-treated.jpg)

