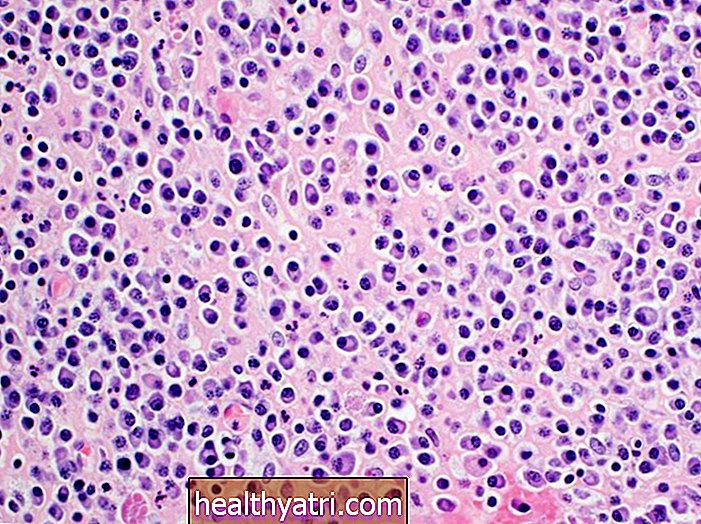
Arseentrioxide - ook bekend als ATO of trisenox - is een antikankerbehandeling voor een subtype van acute myeloïde leukemie dat bekend staat als acute promyelocytische leukemie of APL. Dit leukemie-subtype wordt ook wel "het M3-subtype" van acute myeloïde leukemie genoemd.
De resultaten met ATO bij de behandeling van nieuw gediagnosticeerde patiënten met APL met een laag tot gemiddeld risico waren zeer gunstig. Deze successen hebben ook geleid tot wetenschappelijk onderzoek naar het mogelijke gebruik van ATO bij veel andere kankers dan APL, waaronder niet-leukemie-maligniteiten zoals uitgezaaide darmkanker en de hersentumor, glioblastoma multiforme.
ATO wordt vaak gecombineerd met all-trans retinoïnezuur (ATRA), een retinoïde middel dat wordt gebruikt bij de behandeling van acute promyelocytische leukemie. Retinoïde verbindingen kunnen receptoren op cellen binden om belangrijke acties op cellulaire levenscycli te hebben. Het is aangetoond dat de combinatie van ATRA plus ATO superieur is aan ATRA plus chemotherapie bij de behandeling van patiënten met een standaardrisico met nieuw gediagnosticeerde acute promyelocytische leukemie (APL).
Ariel Skelley / Getty Images
Hoe werkt ATO?
Het werkingsmechanisme van ATO is niet helemaal duidelijk.
In laboratoriumonderzoeken van menselijke promyelocytische leukemiecellen veroorzaakte ATO zowel veranderingen in het uiterlijk van de cellen als breuken in het DNA - die beide wijzen op een proces dat bekend staat als apoptose of geprogrammeerde celdood.
ATO veroorzaakt ook schade aan het fusie-eiwit dat door deze promyelocytische cellen wordt aangemaakt, genaamd Pro-Myelocytic Leukemia / Retinoic Acid Receptor-alpha (PML / RAR alpha). Fusie-eiwitten zijn eiwitten die ontstaan door het samenvoegen van twee of meer genen die oorspronkelijk codeerden voor afzonderlijke eiwitten.
ATO voor APL
ATO is als volgt goedgekeurd voor gebruik bij de behandeling van bepaalde gevallen van acute promyelocytische leukemie of APL:
- Nieuw gediagnosticeerde APL met laag tot gemiddeld risico, waarbij de ATO wordt gebruikt in combinatie met all-trans-retinoïnezuur of ATRA.
- Recidiverende / refractaire APL, bij mensen bij wie eerdere behandelingen een retinoïde en chemotherapie omvatten, in de aanwezigheid van bepaalde genetische veranderingen in de kankercellen - de t (15; 17) -translocatie en / of de aanwezigheid van pro-myelocytische leukemie / retinoïnezuur -receptor-alfa (PML / RAR-alfa) gen.
Het aantal witte bloedcellen (WBC) van een persoon bij presentatie, of op het moment van de eerste evaluatie en diagnose van APL, wordt vaak gebruikt om deze APL-risicogroepen te creëren, waarbij de volgende categorieën worden gebruikt:
- APL met laag of gemiddeld risico = initiële WBC-telling ≤10.000 / microL;
- APL met hoog risico = Initieel aantal leukocyten> 10.000 / microL.
De veiligheid en werkzaamheid van ATO bij kinderen tot 17 jaar zijn niet vastgesteld. Er zijn geen gegevens beschikbaar voor kinderen jonger dan 5 jaar en de gegevens bij oudere kinderen zijn beperkt: in één analyse werden zeven patiënten jonger dan 18 jaar (variërend van 5 tot 16 jaar) behandeld met ATO in de aanbevolen dosis van 0,15 mg / kg / dag, en vijf patiënten bereikten een volledige respons.
De responspercentages van andere AML-subtypen op ATO zijn niet onderzocht. Er zijn onderzoeken met ATO gaande en in de toekomst kunnen er verschillende aanvullende toepassingen van dit middel bij de behandeling van kanker zijn.
ATO + ATRA als inductietherapie
De behandeling van APL verschilt van die van andere soorten AML. De eerste stap van de behandeling, bekend als inductie, is gericht op het bewerkstelligen van remissie en omvat het dwingen van de abnormale cellen van APL, de promyelocyten, om op te groeien tot meer normale cellen.
All-trans-retinoïnezuur, of ATRA, is een niet-chemotherapie-medicijn dat vaak wordt gebruikt voor inductie, omdat het de kwaadaardige promyelocyten dwingt om te rijpen tot neutrofielen. Het is een verbinding die verwant is aan vitamine A. ATRA alleen is echter over het algemeen niet voldoende om remissie te induceren - dat wil zeggen, remissies met alleen ATRA zijn meestal van korte duur en duren slechts enkele maanden. .
ATRA wordt dus meestal gecombineerd met andere middelen om remissie te induceren bij mensen met APL. ATRA in combinatie met op anthracycline gebaseerde chemotherapie is de standaardbehandeling waarvoor de meest uitgebreide klinische ervaring en de grootste hoeveelheid gegevens bestaat.
Er is echter nogal wat interesse in het gebruik van ATO (indien beschikbaar) met ATRA, in plaats van standaard op anthracycline gebaseerde chemotherapie. Aanvankelijk werd dit gezien als een optie voor mensen die op anthracycline gebaseerde chemotherapie niet konden verdragen. Recente klinische onderzoeksgegevens suggereren echter dat de combinatie van ATRA + ATO resultaten kan opleveren die net zo goed, zo niet superieur zijn aan, standaardregimes die ATRA combineren met chemotherapie - bij de juiste patiënttypes.
De meeste ATRA + ATO-gegevens zijn afkomstig van onderzoeken waarin mensen APL met laag risico en APL met gemiddeld risico hadden; er is minder informatie beschikbaar over hoe ATRA + ATO zich zou kunnen verhouden tot ATRA + chemo bij patiënten met hoog risico APL.
Consolidatietherapieën
Net als bij andere typen AML, krijgen patiënten met APL aanvullende behandeling, ruim nadat hun initiële inductietherapie is voltooid, en deze latere behandeling staat bekend als consolidatietherapie.
De specifieke medicatieregimes die worden gebruikt, hangen gedeeltelijk af van de behandelingen die als inductietherapie werden gegeven. Voorbeelden van consolidatietherapieën volgen:
- Anthracycline + ATRA gedurende enkele cycli (verschillende anthracyclines kunnen in verschillende cycli worden gebruikt)
- Anthracycline + cytarabine gedurende ten minste 2 cycli
- ATO gedurende 2 cycli gedurende ongeveer 75 dagen, daarna ATRA + anthracycline gedurende 2 cycli
- ATRA plus ATO voor meerdere cycli
Onderhoudstherapieën
Voor sommige patiënten met APL kan consolidatie worden gevolgd door onderhoudstherapie met ATRA gedurende ten minste een jaar. Soms worden ook lage doses van de chemodrugs 6-mercaptopurine (6-MP) en methotrexaat gegeven.
ATO voor andere ziektecentra - voorlopig onderzoek
Successen met ATO bij de behandeling van APL hebben de wetenschappelijke interesse gewekt in mogelijke rollen voor ATO bij de behandeling van andere maligniteiten.
In veel gevallen is het onderzoek zeer voorlopig, soms beperkt tot ‘reageerbuizen en dierstudies’, maar het feit dat ATO wordt onderzocht in zo veel verschillende ziekteplaatsen en -omgevingen is op zichzelf opmerkelijk.
Een voorbeeld van deze verschillende onderzoeksrichtingen volgt.
Longmetastasen van darmkanker
Adoptieve T-celtherapie is een behandeling die wordt gebruikt om het immuunsysteem te helpen kanker en andere ziekten te bestrijden. T-cellen worden bij de patiënt verzameld en in het laboratorium gekweekt om de kans op een succesvolle reactie van het immuunsysteem te maximaliseren, en vervolgens terug in de patiënt geplaatst om kanker te bestrijden.
In een dierstudie door Wang en collega's gepubliceerd inOncotarget, ATO gecombineerd met cytotoxische T-cellen had een synergetisch effect en verlengde overlevingstijd in een longmetastasemodel van colonkanker. Wang en onderzoekers merkten op dat successen met adoptieve T-celtherapie vaak worden toegeschreven aan de vermindering van regulerende T-cellen en dat ATO positieve effecten kan hebben door deze cellen uit te putten.
Longmetastasen van leverkanker
Gezien het succes van ATO bij APL, vroegen onderzoekers zich af of ATO een vergelijkbaar effect zou kunnen hebben bij leverkanker. Volgens een rapport van Lu en collega's is aangetoond dat infusies van ATO de tumorgroei bij leverkanker remmen.
Bovendien is ATO naar verluidt een effectief geneesmiddel bij de behandeling van longmetastasen van leverkanker met gerelateerde kankerpijn.Lu en collega's merkten op dat studies hebben aangetoond dat ATO de invasie en metastase van leverkankercellen kan remmen door een eiwit genaamd RhoC te remmen en dat RhoC en zijn 'neef-molecuul' ezrin mogelijk betrokken zijn bij de antitumorfunctie van ATO. .
Daarom wilden ze het mechanisme bestuderen van de remming van uitgezaaide leverkankercellen door ATO. Ze gebruikten de expressiepatronen van ezrin voor en na ATO-behandeling als hun observatievenster, en ze ontdekten dat ATO-behandeling de expressie van ezrin bij leverkanker aanzienlijk kan verlagen.
Glioblastoma multiforme
Glioblastoma multiforme, of GBM, is een snelgroeiende, agressieve hersentumor. Dit is het type kanker dat het leven van Ted Kennedy heeft gekost en die bij senator John McCain in 2017 werd vastgesteld.
Van arseentrioxide is gerapporteerd dat het de groei van een breed scala aan solide tumoren, waaronder GBM, remt maar niet vermindert bij een klinisch veilige dosis (1–2 μM). Yoshimura en collega's merkten op dat een lage concentratie (2 μM) arseentrioxide differentiatie van GBM-cellen zou kunnen induceren en ook het effect van andere antikankertherapieën zou kunnen versterken wanneer ze in combinatie in hun muisstudie worden gebruikt, en de hoop is dat dit nieuwe kansen kan bieden. voor toekomstige GBM-therapieën.
Osteosarcoom
Osteosarcoom is een veel voorkomende botkanker en het genezingspercentage is de afgelopen 25 tot 30 jaar niet veel veranderd.
Een proces dat autofagie wordt genoemd, verwijst naar de lysosomen van uw cellen die proteïneaggregaten en beschadigde organellen afbreken en elimineren - in feite het vuilnis buiten zetten om het cytoplasma van de cel schoon te houden.
Autofagiemodulatie wordt beschouwd als een potentiële therapeutische strategie voor osteosarcoom, en de vorige studie gaf aan dat ATO een significante anticarcinogene activiteit vertoont.
Wu en collega's hebben onlangs aangetoond dat ATO de autofagie-activiteit verhoogde in experimentele menselijke osteosarcoomcellen (cellijn MG-63). Interessant is dat het blokkeren van autofagie (met behulp van medicijnen of genetische manipulatie)afgenomende door ATO geïnduceerde celdood, wat suggereert dat ATO autofagische celdood veroorzaakt in MG-63-cellen.
Wu en collega's concludeerden: “Alles bij elkaar genomen tonen deze gegevens aan dat ATO osteosarcoomceldood induceert door overmatige autofagie te induceren, die wordt gemedieerd via de ROS-TFEB-route. De huidige studie biedt een nieuw antitumormechanisme voor ATO-behandeling bij osteosarcoom. "
Een woord van Verywell
In de afgelopen dertig jaar is APL van een zeer dodelijke ziekte naar een zeer geneesbare ziekte gegaan. Behandelingsstrategieën met ATRA, chemotherapie en, meer recentelijk, ATO, worden beschouwd als een hulpmiddel bij deze vooruitgang.
Met deze vorderingen is er echter nog steeds een "onrustig gebied". De veiligheid en werkzaamheid van ATO op de langere termijn kunnen hier in overweging worden genomen, hoewel de tot dusver gerapporteerde langetermijngegevens met ATO + ATRA gunstig waren. Een ander onrustig gebied zou kunnen zijn welke onderhoudstherapieën de voorkeur genieten in het tijdperk van ATRA / ATO.